
Wetenschap
Wat is de reactievergelijking voor ammoniumchloride en water?
Hier is de evenwichtige chemische vergelijking:
nH₄cl (aq) + h₂o (l) ⇌ nH₃ (aq) + h₃o⁺ (aq) + cl⁻ (aq)
Verklaring:
* nH₄cl (aq) vertegenwoordigt ammoniumchloride opgelost in water.
* h₂o (l) vertegenwoordigt vloeibaar water.
* NH₃ (aq) vertegenwoordigt ammoniak opgelost in water.
* h₃o⁺ (aq) vertegenwoordigt hydroniumionen opgelost in water.
* cl⁻ (aq) vertegenwoordigt chloride -ionen opgelost in water.
Belangrijke opmerking: De reactie is omkeerbaar (aangegeven door de dubbele pijlen ⇌), wat betekent dat ammoniak- en hydroniumionen ook kunnen reageren om ammoniumionen en water te vormen. Dit is de reden waarom de oplossing een mengsel van al deze ionen in evenwicht zal bevatten.
De reactie is enigszins zuur Omdat de hydroniumionen die worden geproduceerd door de hydrolyse van ammoniumchloride de oplossing zuurder maken dan zuiver water.
 Chemisch complex kan de uitscheiding van radioactief strontium uit het lichaam verbeteren
Chemisch complex kan de uitscheiding van radioactief strontium uit het lichaam verbeteren Wetenschappers onthullen dynamische koppeling van sterke waterstofbrug
Wetenschappers onthullen dynamische koppeling van sterke waterstofbrug Welke kleur heeft een oplossing op het equivalentiepunt van de titratie?
Welke kleur heeft een oplossing op het equivalentiepunt van de titratie?  Biomining van de elementen van de toekomst
Biomining van de elementen van de toekomst Hoeveel moleculen in zuurstofgas?
Hoeveel moleculen in zuurstofgas?
 Amerikaanse wetenschappers bestuderen de impact van uranium in de Grand Canyon-regio
Amerikaanse wetenschappers bestuderen de impact van uranium in de Grand Canyon-regio Elk gebouw laten meetellen bij het behalen van de emissiedoelstellingen van Australië
Elk gebouw laten meetellen bij het behalen van de emissiedoelstellingen van Australië Sneeuwballenkans op aarde en vroege tekenen van leven
Sneeuwballenkans op aarde en vroege tekenen van leven Proberen het hoofd boven water te houden:hoe het klimaatactieplan van Mumbai tekortschiet
Proberen het hoofd boven water te houden:hoe het klimaatactieplan van Mumbai tekortschiet Welk object kan jou beschrijven?
Welk object kan jou beschrijven?
Hoofdlijnen
- Wat zijn de karakteristieke activiteiten van interfase?
- Wat zijn de drie soorten klonen in eenvoudige vorm?
- Wat zijn aanpassingen aan een grevillea?
- Wat betekent conclusie en discussie in een wetenschap?
- Bevat multicellulair organisme triljoenen cellen?
- Wat is het Atacama-skelet en waarom is het zo controversieel?
- Isoleert het het axon van neuron?
- Nieuwe forensische methode heeft tot doel te voorspellen hoe een persoon eruit ziet op basis van een DNA-monster
- Wat gebeurt er als eerste messager-RNA of transfer-RNA?
- Extreme kou kan de dynamiek van herpesvirusinfecties onthullen
- Volledig inkjet-geprinte op vanadiumdioxide gebaseerde radiofrequentieschakelaars voor flexibele herconfigureerbare componenten

- Norovirusstructuren kunnen helpen bij het ontwikkelen van behandelingen voor voedselvergiftiging
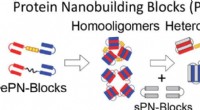
- Wetenschappers ontwikkelen eiwitten die zichzelf assembleren tot supramoleculaire complexen
- Nieuwe methode zet methaan in aardgas bij kamertemperatuur om in methanol

 Zeldzame trofische eieren achter het succes van slangenkopvissen?
Zeldzame trofische eieren achter het succes van slangenkopvissen? Welke woordenschattermen zijn gerelateerd aan energie?
Welke woordenschattermen zijn gerelateerd aan energie?  Waarom oudere vaders meer genetische mutaties doorgeven aan hun nakomelingen
Waarom oudere vaders meer genetische mutaties doorgeven aan hun nakomelingen  Wat is een voorlopig octrooi?
Wat is een voorlopig octrooi?  Waarom lijkt de snelheid van het licht af te nemen in dichtere media?
Waarom lijkt de snelheid van het licht af te nemen in dichtere media?  Beoordeling van biologisch afbreekbare zakken laat zien dat er niet genoeg bekend is om te beoordelen of ze veilig zijn voor het milieu
Beoordeling van biologisch afbreekbare zakken laat zien dat er niet genoeg bekend is om te beoordelen of ze veilig zijn voor het milieu Waarom ziet de zon eruit alsof hij over de lucht beweegt in de hele DA?
Waarom ziet de zon eruit alsof hij over de lucht beweegt in de hele DA?  Welke energie zit er in een helikopter?
Welke energie zit er in een helikopter?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

