
Wetenschap
Is een natriumatoom groter dan siliciumatoom?
Dit is waarom:
* Atomische straal: De atomaire straal is een maat voor de grootte van een atoom. Natrium (NA) bevindt zich in groep 1 (alkali -metalen) en silicium (SI) bevindt zich in groep 14 (koolstofgroep) van het periodiek systeem.
* Periodieke trends: Terwijl u over een periode (van links naar rechts) in het periodiek systeem gaat, neemt de atomaire straal in het algemeen af. Dit komt omdat het aantal protonen in de kern toeneemt en de elektronen dichter bij de kern trekt.
* elektronegativiteit: Natrium heeft een lagere elektronegativiteit dan silicium, wat betekent dat het zijn elektronen minder strak vasthoudt. Dit draagt verder bij dat natrium een grotere atoomradius heeft.
Daarom is een siliciumatoom groter dan een natriumatoom.
 De onderwateroerwouden van de zee geven helderder water
De onderwateroerwouden van de zee geven helderder water Komt natuurlijk? Wandelende wandelende takken gebruiken om natuurlijke selectie en voorspelbaarheid van evolutie te bestuderen
Komt natuurlijk? Wandelende wandelende takken gebruiken om natuurlijke selectie en voorspelbaarheid van evolutie te bestuderen  Sicilië Etna hoger dan ooit na zes maanden activiteit
Sicilië Etna hoger dan ooit na zes maanden activiteit Hoe maak je een druivengelei en oranje feeder van een hanger om Orioles aan te trekken
Hoe maak je een druivengelei en oranje feeder van een hanger om Orioles aan te trekken
Maak een jelly and orange feeder voor je achtertuin om ervoor te zorgen dat orioles verschijnen in je favoriete buitenruimte. Een kleine kom, stokjes, een haak
 Wat zijn de verborgen voordelen van groene infrastructuur?
Wat zijn de verborgen voordelen van groene infrastructuur?
Hoofdlijnen
- Is vlootdiversiteit de sleutel tot duurzame visserij?
- Wanneer een afgebroken deel van het lichaam zich ontwikkelt tot een nakomelingen?
- Jill Brown over waarom bedrijven als ‘kwaadaardig’ worden bestempeld
- Hebben dierencellen een metabolisme met of zonder zuurstof?
- Welke drie vormen kunnen bacteriecellen hebben?
- Wat zijn de drie belangrijkste soorten rna?
- Wat is vervangende klonen?
- Hebben gistcellen membraangebonden organellen?
- Wat doet het exdocriene systeem?
- Een nieuw potentieel alternatief voor muggenbestrijding ontdekt

- Onderzoekers creëren eerste koolstofvezels met uniforme poreuze structuur
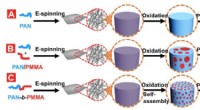
- Materiaalwetenschappers leren hoe ze vloeibare kristallen van vorm kunnen veranderen

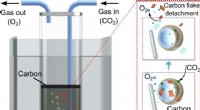
- Vloeibaar metaal bewezen goedkope en efficiënte CO2-converter
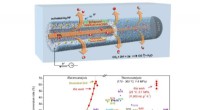
- Nieuwe zilveren holle vezel verhoogt de elektroreductie van CO2
 Triangle 2 plastic containers kunnen een make-over voor het milieu ondergaan
Triangle 2 plastic containers kunnen een make-over voor het milieu ondergaan Hoe de schokveer te bepalen
Hoe de schokveer te bepalen  Drie dingen die we allemaal kunnen leren van mensen die geen smartphones of sociale media gebruiken
Drie dingen die we allemaal kunnen leren van mensen die geen smartphones of sociale media gebruiken Wat is een apparaat dat licht splitst in spectrum voor analyse?
Wat is een apparaat dat licht splitst in spectrum voor analyse?  Wat worden materialen genoemd waarin de elektronen losjes gebonden zijn?
Wat worden materialen genoemd waarin de elektronen losjes gebonden zijn?  Hands-off benadering van siliciumchips
Hands-off benadering van siliciumchips Wat is chemische steno?
Wat is chemische steno?  Hoe laat verliet Apollo 11 de maan?
Hoe laat verliet Apollo 11 de maan?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

