
Wetenschap
Hoeveel atomen van S en O waren aanwezig in de reactie 2SO2 plus O2-2SO3?
2SO₂ + O₂ → 2SO₃
zwavel (s):
* reactanten: 2So₂ bevat 2 * 1 =2 zwavelatomen
* Producten: 2So₃ bevat 2 * 1 =2 zwavelatomen
zuurstof (O):
* reactanten: 2SO₂ bevat 2 * 2 =4 zuurstofatomen
* o₂ Bevat 2 zuurstofatomen
* Totale reactanten: 4 + 2 =6 zuurstofatomen
* Producten: 2SO₃ bevat 2 * 3 =6 zuurstofatomen
Daarom:
* Er zijn 2 zwavelatomen aan beide zijden van de vergelijking.
* Er zijn 6 zuurstofatomen aan beide zijden van de vergelijking.
Sleutelpunt: Een evenwichtige chemische vergelijking zorgt ervoor dat het aantal atomen van elk element hetzelfde is aan zowel de reactant als de productkijker. Dit volgt op de wet van behoud van massa.
 Waarom is het smeltpunt van tafelzout een fysieke eigenschap?
Waarom is het smeltpunt van tafelzout een fysieke eigenschap?  Is FE2O5 een correcte samengestelde formule?
Is FE2O5 een correcte samengestelde formule?  Onderscheid maken tussen een stof en mengsel geven twee voorbeeld van elk?
Onderscheid maken tussen een stof en mengsel geven twee voorbeeld van elk?  Chemische verbinding van Iridium III chloride hexahydraat?
Chemische verbinding van Iridium III chloride hexahydraat?  Wat is de juiste gasvloeistof of vast en als geen smaakgeur?
Wat is de juiste gasvloeistof of vast en als geen smaakgeur?
 Branden zorgden voor verspreiding van graslanden op oude aarde
Branden zorgden voor verspreiding van graslanden op oude aarde 5.9 aardbeving veroorzaakt kleine schade in Australië, geen verwondingen
5.9 aardbeving veroorzaakt kleine schade in Australië, geen verwondingen Noordelijke oceanen hebben ooit CO2 de atmosfeer in gepompt
Noordelijke oceanen hebben ooit CO2 de atmosfeer in gepompt Hoe helpen bossen de atmosfeer in evenwicht te houden?
Hoe helpen bossen de atmosfeer in evenwicht te houden?  Wereldwijd sissend:juli was warmste maand ooit NOAA zegt
Wereldwijd sissend:juli was warmste maand ooit NOAA zegt
Hoofdlijnen
- Zijn er eencellige organismen met chloroplast?
- Is het tijd dat ons begrip van evolutie evolueert?
- Waarom eten zeevogels plastic? Het antwoord stinkt
- Onderzoekers ontdekken een parallel universum in de tomatengenetica
- Produceert sponsachtig bot rode bloedcellen?
- Welke banen zijn in San Antonio Texas beschikbaar als u een diploma in biologie heeft?
- Hoe zijn computervirussen vergelijkbaar met en verschillend van biologische virussen?
- Waarom worden virussen als biologisch belangrijk beschouwd?
- Wat is de definitie van intern en extern?
- Chemische ingenieurs ontwikkelen nieuwe klasse multifunctioneel precisiepolymeer

- MasSpec-pen voor nauwkeurige kankerdetectie tijdens operaties

- Visualisatie van moleculaire beweging van gesubstitueerd 9-fosfaanthraceen

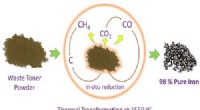
- Strijkijzer uit printerafvaltoner trekken
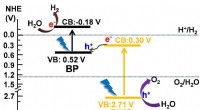
- Ultradunne zwarte fosfor voor door zonne-energie aangedreven waterstofeconomie
 Hoe spitsmuizen, mollen en woelmuizen te identificeren
Hoe spitsmuizen, mollen en woelmuizen te identificeren  Hoe beïnvloedt fossiele brandstoffen kalksteen?
Hoe beïnvloedt fossiele brandstoffen kalksteen?  Wat de wereld kan leren van de verwoestende overstromingen in Pakistan
Wat de wereld kan leren van de verwoestende overstromingen in Pakistan  Wat is de wetenschappelijke classificatie van wezelsoorten?
Wat is de wetenschappelijke classificatie van wezelsoorten?  Hoe je op een ruimtesteen jaagt
Hoe je op een ruimtesteen jaagt  Als een object beweegt met een welke snelheid, zal het dit blijven doen, tenzij Force erop handelt?
Als een object beweegt met een welke snelheid, zal het dit blijven doen, tenzij Force erop handelt?  Wetenschappers fabriceren een dubbel PH-responsief slim afgiftesysteem voor pesticiden
Wetenschappers fabriceren een dubbel PH-responsief slim afgiftesysteem voor pesticiden Waarom zijn de bergen van de Himalaya een omgekeerde fout?
Waarom zijn de bergen van de Himalaya een omgekeerde fout?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

