
Wetenschap
Wat is het snelst bewegende gasmolecuul?
Dit is waarom:
* Kinetische moleculaire theorie: De snelheid van gasmoleculen is direct gerelateerd aan hun temperatuur. Hoe hoger de temperatuur, hoe sneller de moleculen bewegen.
* Moleculaire massa: Lichtere moleculen bewegen sneller dan zwaardere op dezelfde temperatuur.
Om het snelst bewegende gasmolecuul te bepalen, zou u moeten:
1. Ken de temperatuur: Hoe hoger de temperatuur, hoe sneller alle moleculen zullen bewegen.
2. Denk aan de moleculaire massa: Lichte moleculen zoals waterstof (H₂) zullen over het algemeen sneller bewegen dan zwaardere moleculen zoals zuurstof (O₂).
Voorbeeld:
Bij een gegeven temperatuur zal waterstofgas (H₂) de snelst bewegend zijn omdat het de laagste moleculaire massa heeft. Als u echter de temperatuur van een zwaarder gas zoals Xenon (XE) verhoogt, kan het mogelijk sneller bewegen dan waterstof bij een lagere temperatuur.
Key Takeaway: Het snelst bewegende gasmolecuul hangt af van zowel temperatuur als moleculaire massa.
 Wat is het verschil tussen pangaea en panthalasa?
Wat is het verschil tussen pangaea en panthalasa?  Wanneer een vloeistof verandert in gas, wat voor soort fysieke verandering heeft zich voorgedaan?
Wanneer een vloeistof verandert in gas, wat voor soort fysieke verandering heeft zich voorgedaan?  Welke vorm wordt materie het meest aangetroffen uit elementen, verbindingen en mengsels?
Welke vorm wordt materie het meest aangetroffen uit elementen, verbindingen en mengsels?  Wat is de chemische formule van cadaverine?
Wat is de chemische formule van cadaverine?  Cement versus beton:hun verschillen, en kansen voor duurzaamheid
Cement versus beton:hun verschillen, en kansen voor duurzaamheid
Hoofdlijnen
- Wat gebeurt er met het aantal witte bloedcellen tijdens een infectie?
- Hoe is het mitochondriën en het spijsverteringssysteem vergelijkbaar?
- Wat is de naam van cel die neurotransmitters vrijgeeft?
- Wetenschappers ontdekken de mysteries van hoe virussen evolueren
- Welke bloedcellen worden in bepaalde botten in uw lichaam gemaakt?
- Wat is de naam van alle wetenschapper?
- Wat is de meest voorkomende chromosomale afwijking bij mensen?
- Wat voor soort biome is Abbotsford?
- Onderzoek suggereert dat cellen een verborgen communicatiesysteem bezitten
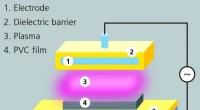
- Plasmabehandeling vermindert de migratie van weekmakers uit bloedzakken
- Onderzoekers infuseren bacteriën met zilver om de energie-efficiëntie in brandstofcellen te verbeteren

- Van spoor wisselen:Omgekeerde elektronen gaan door natuurlijke zonnecellen

- Op mosselen geïnspireerde lijm kan op een dag foetale chirurgie veiliger maken

- Programmeerbare druppelmanipulatie door een robot met magnetische activering

 Hoe is versnelling in oceaangolven?
Hoe is versnelling in oceaangolven?  Is the Betelgeuse and stars different colors?
Is the Betelgeuse and stars different colors?  Wat produceert golven met kleine amplitudes?
Wat produceert golven met kleine amplitudes?  Herdefiniëren van kennis van ouderen door de geschiedenis heen
Herdefiniëren van kennis van ouderen door de geschiedenis heen Waarom worden organische oplosmiddelen niet -polair oplosmiddel genoemd?
Waarom worden organische oplosmiddelen niet -polair oplosmiddel genoemd?  Microscopische computers:de draden van de toekomst kunnen gemaakt zijn van moleculen
Microscopische computers:de draden van de toekomst kunnen gemaakt zijn van moleculen Wat zijn goede dingen over biomassa -energie?
Wat zijn goede dingen over biomassa -energie?  Hoeveel elektronen in Scandium -ion?
Hoeveel elektronen in Scandium -ion?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

