
Wetenschap
Wat is de moleculaire en netto ionische vergelijking van bariumhydroxide -hydrocyaninezuur?
1. Moleculaire vergelijking
* reactanten: Bariumhydroxide (BA (OH) ₂) en hydrocyaniczuur (HCN)
* Producten: Barium cyanide (BA (CN) ₂) en water (H₂o)
Moleculaire vergelijking:
Ba (oh) ₂ (aq) + 2hcn (aq) → ba (cn) ₂ (aq) + 2h₂o (l)
2. Netto ionische vergelijking
* Identificeer de sterke elektrolyten: Bariumhydroxide, hydrocyaninezuur en bariumcyanide zijn sterke elektrolyten.
* Schrijf de volledige ionische vergelijking: Breek de sterke elektrolyten in hun ionen af.
* Annuleer de toeschouwersionen: Toeschouwersionen verschijnen aan beide zijden van de vergelijking en nemen niet deel aan de reactie.
Volledige ionische vergelijking:
Ba²⁺ (aq) + 2oH⁻ (aq) + 2h⁺ (aq) + 2cn⁻ (aq) → ba²⁺ (aq) + 2cn⁻ (aq) + 2h₂o (l)
Netto ionische vergelijking:
2OH⁻ (aq) + 2H⁺ (aq) → 2h₂o (l)
Vereenvoudigde netto ionische vergelijking:
oh⁻ (aq) + h⁺ (aq) → h₂o (l)
Belangrijke opmerking: Hydrocyaniczuur (HCN) is een zwak zuur, maar het wordt in dit geval behandeld als een sterke elektrolyt omdat de reactie wordt aangedreven door de vorming van water.
 Turbulentie door topografie van de zeebodem kan een langlopende vraag over oceaancirculatie verklaren
Turbulentie door topografie van de zeebodem kan een langlopende vraag over oceaancirculatie verklaren Uitbreiding wind- en zonne-energie te langzaam om klimaatverandering te stoppen
Uitbreiding wind- en zonne-energie te langzaam om klimaatverandering te stoppen NASA kijkt naar tropische storm Son-Tinh die het eiland Hainan treft, China
NASA kijkt naar tropische storm Son-Tinh die het eiland Hainan treft, China Waarom het onschadelijk maken van koolstofbommen een veelbelovende nieuwe agenda biedt voor het aanpakken van klimaatverandering
Waarom het onschadelijk maken van koolstofbommen een veelbelovende nieuwe agenda biedt voor het aanpakken van klimaatverandering Satellieten volgen verdwijnend Antarctisch ijs
Satellieten volgen verdwijnend Antarctisch ijs
Hoofdlijnen
- Welk punt in mitose vormt een splitsing in de vorm?
- Wat is de belangrijkste functie van oksel?
- Wat voor soort wetenschap neemt u in het 12e leerjaar?
- Van 'boops' tot 'unks', hoe wetenschappers visgeluiden gebruiken om onderwaterecosystemen te behouden
- Welk type reproductie treedt op wanneer zich een kleine bult of knop vormt op oudercel en vervolgens afbreekt om een nieuwe cel te vormen?
- Een incubator laten groeien Bacteriën
- Gewelddadige dromen kunnen een aanwijzing zijn waarom dromen zijn geëvolueerd, zeggen onderzoekers
- Celmembraan is naar een cel als nucleair?
- Het homeostatische mechanisme bij mensen dat de pH van de bloedreguleert, hangt af van de feedback van informatie uit?
- Polymeren springen door hoepels op weg naar duurzame materialen

- Samengestelde metalen schuimen nemen de hitte, dichter bij wijdverbreide toepassingen komen

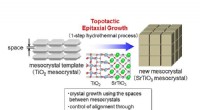
- Fotokatalysator maakt waterstofproductie 10 keer efficiënter
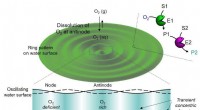
- Regeling in de tijd van chemische reacties met alleen hoorbaar geluid
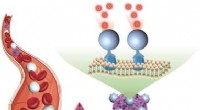
- Directe detectie van circulerende tumorcellen in bloedmonsters
 Hoe verschilt lichte energie van zowel geluids- als warmte -energie?
Hoe verschilt lichte energie van zowel geluids- als warmte -energie?  Wat voornamelijk samengesteld uit ijsstof en gas rondom de zon?
Wat voornamelijk samengesteld uit ijsstof en gas rondom de zon?  Waarom gebruik je modellen om de natuur te beschrijven?
Waarom gebruik je modellen om de natuur te beschrijven?  Wat is het eenvoudigste deel van een compound?
Wat is het eenvoudigste deel van een compound?  De omgeving verbeteren:wanneer oplossingen problemen worden
De omgeving verbeteren:wanneer oplossingen problemen worden Astrofysici leggen een nieuwe klasse van voorbijgaande objecten vast
Astrofysici leggen een nieuwe klasse van voorbijgaande objecten vast Zal de massa van een object worden gegooid door een katapult van invloed op de afstand?
Zal de massa van een object worden gegooid door een katapult van invloed op de afstand?  Wat gebeurt er als natriumfosfaat wordt gemengd met kopersulfaat?
Wat gebeurt er als natriumfosfaat wordt gemengd met kopersulfaat?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

