
Wetenschap
Water lost veel ionische en moleculaire verbindingen op vanwege zijn wat?
Dit is waarom:
* Water is een polair molecuul: Het zuurstofatoom in water is elektronegatiefer dan de waterstofatomen, wat betekent dat het elektronen sterker aantrekt. Dit creëert een gedeeltelijke negatieve lading op de zuurstof- en gedeeltelijke positieve ladingen op de hydrogenen, waardoor het molecuul polair is.
* ionische verbindingen worden bij elkaar gehouden door elektrostatische krachten: Deze krachten zijn sterk, maar ze kunnen worden verstoord door polaire moleculen zoals water. De gedeeltelijk negatieve zuurstof in water trekt de positieve ionen in de ionische verbinding aan en de gedeeltelijk positieve hydrogenen trekken de negatieve ionen aan. Deze aantrekkingskracht verzwakt de elektrostatische krachten die de ionische verbinding tegen elkaar houden, waardoor deze oplost.
* Polaire moleculen lossen op in polaire oplosmiddelen: Water is een polair oplosmiddel en kan andere polaire moleculen zoals suikers en alcoholen oplossen. De gedeeltelijke ladingen op het watermolecuul interageren met de gedeeltelijke ladingen op de polaire moleculen, waardoor ze oplossen.
Samenvattend: Met de polariteit van het water kan het interageren met zowel ionische als polaire moleculen, waardoor hun bindingen worden verstoord en oplost.
 Welke van de volgende is waar, een ondoorzichtige radio -substantie?
Welke van de volgende is waar, een ondoorzichtige radio -substantie?  Wat is de chemische formule voor fosfor III -oxide?
Wat is de chemische formule voor fosfor III -oxide?  Wat is het oxidatiegetal van Cl in PtCl42?
Wat is het oxidatiegetal van Cl in PtCl42?  Is 2SO2 plus o2 gelijk aan 2SO3 een verbrandingsreactie Waarom of waarom niet?
Is 2SO2 plus o2 gelijk aan 2SO3 een verbrandingsreactie Waarom of waarom niet?  Hoeveel fluoratomen zijn er in elk molecuul Disulfur decafluoride?
Hoeveel fluoratomen zijn er in elk molecuul Disulfur decafluoride?
 Chinese stad plukt door het puin na recordregens 33 . doden
Chinese stad plukt door het puin na recordregens 33 . doden GPS is niet alleen meer voor roadtrips
GPS is niet alleen meer voor roadtrips Effecten van een modderstroom
Effecten van een modderstroom  Wat is het verschil tussen het liefhebben van dingen en niets dat in vormgrootte leeft?
Wat is het verschil tussen het liefhebben van dingen en niets dat in vormgrootte leeft?  Koraalverlies op Palmeilanden gaat lang vooraf aan massaverbleking in 2016 op Great Barrier Reef
Koraalverlies op Palmeilanden gaat lang vooraf aan massaverbleking in 2016 op Great Barrier Reef
Hoofdlijnen
- Wat is het tegenovergestelde van prokaryotisch?
- Door alles te proberen, leert de roofzuchtige zeeslak wat hij niet mag eten
- Wat doet ADP in de biologie?
- Kuifduiven gebruiken veren om alarm te slaan
- Hoe verschilt cytokinese in plantencellen van menselijke en dierlijke cellen?
- Hoe bacteriën worden geclassificeerd op de bases van flagella?
- Waarom is een kloon een exacte kopie van u?
- Onderzoekers onthullen hoe mirte-roestziekteverwekker een waardplant binnendringt
- Als een lichaamscel 22 chromosomen heeft, wat zou de telling voor reproductieve cellen zijn?
- Onderzoek onthult structuur van humane endogene reverse transcriptase
- Onderzoekers ontdekken dat ruimte tussen polymeerketens de energieconversie beïnvloedt

- Niet te nat, niet te droog - met plasma behandelde brandstofcel doet het precies goed

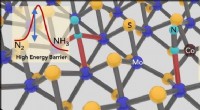
- Ammoniaksynthese gemakkelijk gemaakt met 2D-katalysator
- Onderzoekers creëren een effectievere hydrogel voor het genezen van wonden

 Hoe los je op voor de grootte van snelheid?
Hoe los je op voor de grootte van snelheid?  Hoe een polymeerklei te vormen?
Hoe een polymeerklei te vormen?  Welk enzym is nodig om transcriptie te laten plaatsvinden?
Welk enzym is nodig om transcriptie te laten plaatsvinden?  Gezichten van dominantie:waarom de gezichten van vrouwen en mannen anders worden waargenomen door liberale conservatieven
Gezichten van dominantie:waarom de gezichten van vrouwen en mannen anders worden waargenomen door liberale conservatieven  Nieuwe gel beschermt eieren - en misschien ooit koppen - tegen schade
Nieuwe gel beschermt eieren - en misschien ooit koppen - tegen schade De eerste wetenschappelijke databank van Indonesië is een stap in de richting van het versterken van open data-praktijken
De eerste wetenschappelijke databank van Indonesië is een stap in de richting van het versterken van open data-praktijken De hoeveelheid werk die door een warmtemotor is gedaan, is gelijk aan de thermische energie.
De hoeveelheid werk die door een warmtemotor is gedaan, is gelijk aan de thermische energie.  Wat gebeurt er met de zonne -energie die planeten ontvangen van de zon wanneer u verder gaat in het systeem?
Wat gebeurt er met de zonne -energie die planeten ontvangen van de zon wanneer u verder gaat in het systeem?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

