
Wetenschap
Waarom is de pH voor de reactie van natriumoxide en water hoger dan calciumwater?
Natriumoxide (Na₂o) en water
* reactie: Natriumoxide reageert krachtig met water om natriumhydroxide (NaOH) te vormen:
Na₂o + H₂o → 2naOH
* NaOH is een sterke basis: Natriumhydroxide dissocieert volledig in water, waardoor hydroxide -ionen (OH⁻) worden vrijgeeft die de oplossing zeer alkalisch maken, wat resulteert in een hoge pH.
calciumoxide (Cao) en water
* reactie: Calciumoxide reageert met water om calciumhydroxide (Ca (OH) ₂) te vormen:
Cao + H₂o → CA (OH) ₂
* ca (oh) ₂ is een sterke basis maar minder oplosbaar: Calciumhydroxide is ook een sterke basis, wat betekent dat het ook hydroxide -ionen (OH⁻) in oplossing vrijgeeft. Het is echter minder oplosbaar in water dan natriumhydroxide. Dit betekent dat minder Ca (OH) ₂ oplost, waardoor minder oh⁻ionen worden geproduceerd in vergelijking met NaOH in een vergelijkbare oplossing.
Waarom natriumoxide -oplossing een hogere pH heeft
De hogere pH van de natriumoxide -oplossing is te wijten aan:
* Hogere concentratie OH⁻: Omdat natriumhydroxide meer oplosbaar is, produceert het een hogere concentratie hydroxide -ionen in oplossing, waardoor de oplossing alkalischer wordt.
* sterkere basis: Zowel natriumhydroxide als calciumhydroxide zijn sterke basen, maar hun oplosbaarheidsverschil beïnvloedt de concentratie van de hydroxide -ionen aanzienlijk.
Samenvattend: Hoewel zowel natriumoxide als calciumoxide reageren met water om sterke basen te vormen, leidt de hogere oplosbaarheid van natriumhydroxide tot een hogere concentratie hydroxide -ionen, resulterend in een hogere pH vergeleken met de calciumoxide -oplossing.
 Onverwoestbaar virus onthult geheim voor het maken van ongelooflijk duurzame materialen
Onverwoestbaar virus onthult geheim voor het maken van ongelooflijk duurzame materialen Wat is het neerslag wanneer kaliumbromide en zilvernitraat worden gemengd?
Wat is het neerslag wanneer kaliumbromide en zilvernitraat worden gemengd?  Wat is de formule voor natriumwaterstofsulfaat?
Wat is de formule voor natriumwaterstofsulfaat?  Wat is de molariteit van een onbekend zuur als 40,5 ml kan worden getitreerd tot het eindpunt met 20,5.2250 M NaOH?
Wat is de molariteit van een onbekend zuur als 40,5 ml kan worden getitreerd tot het eindpunt met 20,5.2250 M NaOH?  Wat is het verwachte aantal valentie -elektronen voor een groep 3 A -element?
Wat is het verwachte aantal valentie -elektronen voor een groep 3 A -element?
 Onderzoek onderzoekt hoe bevooroordeelde percepties de erosie van democratische waarden in de VS kunnen veroorzaken
Onderzoek onderzoekt hoe bevooroordeelde percepties de erosie van democratische waarden in de VS kunnen veroorzaken  Alle levende en niet -levende elementen op een bepaalde plaats worden een (n) genoemd?
Alle levende en niet -levende elementen op een bepaalde plaats worden een (n) genoemd?  Zullen veranderingen in het klimaat de Arctische en subarctische gebieden van zoogdieren uitroeien?
Zullen veranderingen in het klimaat de Arctische en subarctische gebieden van zoogdieren uitroeien?  Welke natuurkracht werkt over de langste afstand?
Welke natuurkracht werkt over de langste afstand?  Blauwe bakken lopen over van Amazon- en Walmart-dozen. Maar waren eigenlijk minder aan het recyclen
Blauwe bakken lopen over van Amazon- en Walmart-dozen. Maar waren eigenlijk minder aan het recyclen
Hoofdlijnen
- Wat zijn borstcellen?
- Welke beschrijft het beste hoe ons begrip van DNA en erfelijke eigenschappen in de loop van de tijd is veranderd?
- Een verklaring van het skeletsysteem
- Wanneer u wetenschappelijke methoden gebruikt om een probleem op te lossen, is wetenschapper waarschijnlijk dat het doet na het vormen van hypothese?
- Wat is het doel van een lab?
- Is rijst een voorbeeld van epigeale kieming?
- Wat is kwantitave onherkenning in het genen?
- Natuurbeschermers bevestigen de vierde aanval van grijze wolven in Grand County in Colorado
- Waarom zijn er twee van elk chromosoom in een normaal karyotype?
- Wetenschappers hopen op een nieuwe ionenval om 's werelds meest nauwkeurige massaspectrometer te creëren

- Een venster voor traploos ladingtransport in organische halfgeleiders
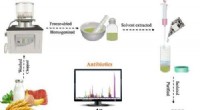
- Sporen van meerdere klassen antibiotica in voedingsmiddelen detecteren
- Chemici slagen erin aminoalcoholen te synthetiseren door gebruik te maken van licht
- Modern poreus materiaal lijkt op XIV-eeuws Alhambra-mozaïek

 De evolutie van Maxwell-knopen volgen
De evolutie van Maxwell-knopen volgen De nacht was zo donker tegen die tijd dat het tot de ochtend zou zijn en welk licht we leken meer uit de rivier te komen dan hemeren in hun dompel die op een paar gereflecteerde sterren werd geslagen. De?
De nacht was zo donker tegen die tijd dat het tot de ochtend zou zijn en welk licht we leken meer uit de rivier te komen dan hemeren in hun dompel die op een paar gereflecteerde sterren werd geslagen. De?  Wat gebeurt er met de afstand tussen Andromeda Galaxy en Melkweg?
Wat gebeurt er met de afstand tussen Andromeda Galaxy en Melkweg?  Hoeveel voet water vertegenwoordigt 15 PSI?
Hoeveel voet water vertegenwoordigt 15 PSI?  Elektrische fietsen zoemen binnenkort langs de paden van het nationale park
Elektrische fietsen zoemen binnenkort langs de paden van het nationale park Lagen cellen die vergelijkbaar zijn in structuur en perfom een bepaalde fuctie die wordt genoemd?
Lagen cellen die vergelijkbaar zijn in structuur en perfom een bepaalde fuctie die wordt genoemd?  Welke planeet heeft een dag ongeveer even lange aarde?
Welke planeet heeft een dag ongeveer even lange aarde?  Welke 3 dingen die erosie en afzetting veroorzaken?
Welke 3 dingen die erosie en afzetting veroorzaken?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

