
Wetenschap
Welke elementen zouden waarschijnlijk op chloor zijn?
* Vergelijkbare elektronische configuratie: Alle halogenen hebben zeven elektronen in hun buitenste schaal, waardoor ze een hoge elektronegativiteit hebben en een neiging om één elektron te krijgen om een stabiele octetconfiguratie te bereiken.
* Soortgelijke chemische eigenschappen: Ze hebben de neiging om ionische verbindingen te vormen met metalen en covalente verbindingen met niet -metalen. Ze vormen ook gemakkelijk diatomaire moleculen (zoals CL2, BR2, enz.).
* Vergelijkbare fysieke eigenschappen: Naarmate je de halogeengroep doorgaat, worden de elementen minder reactief, hebben ze hogere smelt- en kookpunten en wordt hun kleur dieper.
Daarom zijn de elementen waarschijnlijk als chloor:
* fluor (f): Zeer reactief, lichtgeel gas.
* Bromine (Br): Een roodbruine vloeistof bij kamertemperatuur.
* jodium (i): Een donkerpaarse vaste stof die gemakkelijk sublimeert.
* astatine (AT): Een radioactief, uiterst zeldzaam element.
Opmerking: Hoewel astatine ook een halogeen is, maakt de radioactieve aard het minder op chloor in termen van dagelijkse chemische eigenschappen.
 Goedkoop, draagbare detector identificeert ziekteverwekkers in minuten
Goedkoop, draagbare detector identificeert ziekteverwekkers in minuten Voorgestelde technische methode kan gebouwen en bruggen veiliger maken
Voorgestelde technische methode kan gebouwen en bruggen veiliger maken Wordt de gas uit wanneer gekoeld?
Wordt de gas uit wanneer gekoeld?  Ontworpen moleculen verwijderen selectief ongewenste ionen uit complexe oplossingen voor energieproductie
Ontworpen moleculen verwijderen selectief ongewenste ionen uit complexe oplossingen voor energieproductie 10 soorten fysieke verandering
10 soorten fysieke verandering
 Wat is een metafoor voor chloroplast?
Wat is een metafoor voor chloroplast?  Hoe is het leven op aarde ontstaan? Atmosferische nevel zou de sleutel kunnen zijn geweest
Hoe is het leven op aarde ontstaan? Atmosferische nevel zou de sleutel kunnen zijn geweest  Sanibel Island, Florida Scheitips
Sanibel Island, Florida Scheitips  Stijgende zeeën zullen miljoenen mensen verdrijven - en Australië moet er klaar voor zijn
Stijgende zeeën zullen miljoenen mensen verdrijven - en Australië moet er klaar voor zijn Hoe rustige ruimtes mensen kunnen helpen zich kalm en ontspannen te voelen in steden
Hoe rustige ruimtes mensen kunnen helpen zich kalm en ontspannen te voelen in steden
Hoofdlijnen
- Een nieuw hulpmiddel voor de identificatie van niet-coderend RNA van planten
- Welk type redeneermethode gebruiken wetenschappers?
- Wat zijn wetenschapsvragen?
- Wat zijn de kenmerken van blad- en uiencellen van wangcellen?
- Wat is de semifluidmatrix in het interieur van een cel?
- Welke organel combineert eiwitten?
- Welk type axon verspreidt een actiepotentieel sneller?
- Toezichthouders overwegen hoe ze de zuidelijke kreeft uit New England kunnen redden
- Welk organisme is waarschijnlijker te vinden in amber een kever of konijn?
- Industrieel afval gebruiken als isolatie voor gebouwen

- Nemen van de inlandse superfood mainstream van Australië

- Een nieuwe gids voor ontdekkingsreizigers van de submicroscopische wereld in ons

- Begrijpen wat zwart pigment zwart maakt

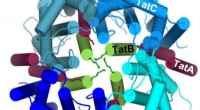
- Biochemici onderzoeken het transport van grote eiwitten door bacteriële celmembranen
 Chemici synthetiseren miljoenen eiwitten die niet in de natuur voorkomen
Chemici synthetiseren miljoenen eiwitten die niet in de natuur voorkomen Lyfts-aandelen stijgen als investeerders wedden op de toekomst van ride-hailing
Lyfts-aandelen stijgen als investeerders wedden op de toekomst van ride-hailing Hardware-software co-design-aanpak kan neurale netwerken minder energieverslindend maken
Hardware-software co-design-aanpak kan neurale netwerken minder energieverslindend maken Wat het coronavirus ons vertelt over de klimaatverandering op de 50e verjaardag van Earth Day
Wat het coronavirus ons vertelt over de klimaatverandering op de 50e verjaardag van Earth Day  Gebruiken mensen radiatoren echt om stills te maken?
Gebruiken mensen radiatoren echt om stills te maken?  Wordt kinetische energie toeneemt als massa is dat ture?
Wordt kinetische energie toeneemt als massa is dat ture?  Hoe werk je de energiebedrag in een knapperig?
Hoe werk je de energiebedrag in een knapperig?  Wetenschappers werpen licht op mysterie van donkere materie
Wetenschappers werpen licht op mysterie van donkere materie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

