
Wetenschap
Waarom worden voorvoegsels gebruikt bij het benoemen van covalente verbindingen?
Dit is de reden waarom voorvoegsels nodig zijn en hoe ze werken:
* Duidelijkheid en specificiteit: Zonder voorvoegsels zou het onmogelijk zijn om onderscheid te maken tussen verschillende covalente verbindingen met verschillende aantallen atomen. CO en CO2 zijn bijvoorbeeld beide verbindingen van koolstof en zuurstof, maar ze hebben zeer verschillende eigenschappen en formules. Voorvoegsels zoals "mono-" en "di-" stellen ons in staat om deze verbindingen duidelijk te identificeren als koolmonoxide en koolstofdioxide.
* Consistentie en standaardisatie: Voorvoegsels bieden een gestandaardiseerd systeem voor het benoemen van covalente verbindingen. Dit maakt het voor chemici gemakkelijker om te communiceren en elkaar te begrijpen.
* Inzicht in de moleculaire structuur: De voorvoegsels in de naam van een covalente verbinding komen rechtstreeks overeen met het aantal atomen in het molecuul. Dit helpt de structuur te visualiseren en de binding binnen de verbinding te begrijpen.
Hier is een uitsplitsing van de gemeenschappelijke voorvoegsels die worden gebruikt in covalente samengestelde nomenclatuur:
| Voorvoegsel | Nummer |
| --- | --- |
| Mono- | 1 |
| Di- | 2 |
| Tri- | 3 |
| Tetra- | 4 |
| Penta- | 5 |
| Hexa- | 6 |
| Hepta- | 7 |
| Octa- | 8 |
| Nona- | 9 |
| Deca- | 10 |
Voorbeelden:
* CO2: Koolstofdioxide (DI- duidt op twee zuurstofatomen)
* N2O4: Dinitrogene tetroxide (di- duidt op twee stikstofatomen, tetra- duidt op vier zuurstofatomen)
* PCL5: Fosfor pentachloride (penta- duidt op vijf chlooratomen)
Concluderend zijn voorvoegsels essentieel voor het benoemen van covalente verbindingen omdat ze duidelijkheid, consistentie en een directe weergave van de moleculaire structuur bieden.
 Hoe AI het water in stedelijke rivieren zuivert
Hoe AI het water in stedelijke rivieren zuivert  Mammoetjagers - weg met een gejammer of een knal?
Mammoetjagers - weg met een gejammer of een knal?  Orkanen kunnen landinwaarts enorme schade aanrichten, maar noodplannen richten zich op kusten
Orkanen kunnen landinwaarts enorme schade aanrichten, maar noodplannen richten zich op kusten Wetenschappers synthetiseren onderzoek, model voor kustbepantsering evalueren
Wetenschappers synthetiseren onderzoek, model voor kustbepantsering evalueren Wat zijn natuurlijke hulpbronnen?
Wat zijn natuurlijke hulpbronnen?
Hoofdlijnen
- Waarom stinkt de stinkplant?
- Noem de zeven eigenschappen die alle levende organismen delen?
- Welke drie woorden gebruik je voor de hypothese?
- Wat is het doel in het laboratoriumrapport?
- Wat baseren biologen hun in geloof evolutietheorie?
- Hoe heeft Florida niet gereageerd op een epizoötische koraalziekte en wat volgt?
- Hoe zijn gespecialiseerde cellen van xyleem en floëem geschikt voor hun functies?
- Fatale hechting:hoe pathogene bacteriën zich aan het slijmvlies hechten en afschilfering voorkomen
- Wat moet een cel uitbreiden tijdens actief transport om de beweging van de inhoud te bereiken?
- Alternatief voor stikstof:Zuurstofplasma kan de eigenschappen van elektrodematerialen verbeteren
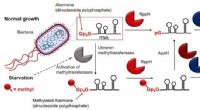
- Ontdekking van geheel nieuwe klasse RNA-caps in bacteriën
- Moleculaire structuren in meer detail analyseren
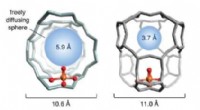
- Wetenschappers zetten methaan bij kamertemperatuur om in methanol
- Zuurstof geven aan de kwestie van luchtkwaliteit

 Bacteriën zijn de enige organismen die kunnen?
Bacteriën zijn de enige organismen die kunnen?  Slimmere steden, slimmer leven
Slimmere steden, slimmer leven Chemici verkregen nieuwe verbinding voor moleculaire machines
Chemici verkregen nieuwe verbinding voor moleculaire machines Hoe snelheid verandert in verschillende media?
Hoe snelheid verandert in verschillende media?  Effecten van de Waterstof Bomb
Effecten van de Waterstof Bomb Welk type aseksuele reproductie gebruiken planten?
Welk type aseksuele reproductie gebruiken planten?  Landbouw met een hoog rendement kost het milieu minder dan eerder werd gedacht - en zou habitats kunnen sparen
Landbouw met een hoog rendement kost het milieu minder dan eerder werd gedacht - en zou habitats kunnen sparen Zou de asteroïde Ryugu een overblijfsel kunnen zijn van een uitgestorven komeet?
Zou de asteroïde Ryugu een overblijfsel kunnen zijn van een uitgestorven komeet?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

