
Wetenschap
Is zwavel dichloride oplosbaar in water?
* Reactiviteit met water: SCL₂ reageert heftig met water. Deze reactie produceert zwaveldioxide (SO₂) en zoutzuur (HCL):
SCL₂ + 2 H₂o → So₂ + 2 HCl
* polariteit: Water is een zeer polair molecuul, terwijl SCL₂ een niet -polair molecuul is. "Zoals oplost zoals" is een algemene vuistregel in de chemie. Niet -polaire stoffen lossen in niet -polaire oplosmiddelen op en polaire stoffen lossen op in polaire oplosmiddelen.
* Vorming van een emulsie: Zelfs als een kleine hoeveelheid SCL₂ in contact zou komen met water, zou het niet oplossen. In plaats daarvan zou het waarschijnlijk snel reageren, warmte genereren en een corrosief mengsel van SO₂ en HCL produceren.
Belangrijke opmerking: Vanwege de gevaarlijke reactie met water moet zwaveldichloride met extreme voorzichtigheid worden afgehandeld.
Hoofdlijnen
- Klier die een factor scheidt, zorgt ervoor dat T-cellen volwassen worden?
- Geautomatiseerde machine learning-robot ontsluit nieuw potentieel voor genetisch onderzoek
- Wetenschappers ontdekken hoe cellen reageren op vasten
- Nieuwe detectietechnieken kunnen droogtetolerantie in oude gewassen detecteren en kunnen nieuwe fokprogramma's informeren
- Hoeveel verschillende soorten gameten kan een individuele vorm van DDGGWW?
- Wat is een wetenschapper die de hersenen bestudeert?
- Wat is eetwetenschap?
- Wat is inconsisterie?
- Welke soorten organismen doen stikstoffixatie?
- Het temmen van defecte poreuze materialen voor robuuste en selectieve heterogene katalyse
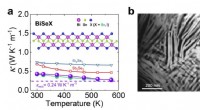
- Extreem lage thermische geleidbaarheid in 1-D zachte kettingstructuur
- Make like a leaf:onderzoekers ontwikkelen methode om koolstofdioxide om te zetten

- Ontwerpaanpak ontwikkeld voor nieuwe katalysatoren voor energieconversie en -opslag

- Onderzoekers ontwikkelen op smartphone gebaseerde ovulatietest
 Japanse ingenieurs maken robot die pushups doet,
Japanse ingenieurs maken robot die pushups doet,  Welke wrijving treedt op wanneer een object door een vloeistof of gas beweegt?
Welke wrijving treedt op wanneer een object door een vloeistof of gas beweegt?  Welke elementen zijn in loodchloride?
Welke elementen zijn in loodchloride?  Moleculaire knoop wint record voor 's werelds strakste
Moleculaire knoop wint record voor 's werelds strakste Is de goede warmtestraler een glanzend verzilverd oppervlak of een wit oppervlak?
Is de goede warmtestraler een glanzend verzilverd oppervlak of een wit oppervlak?  Nanodeeltjes als mogelijke oplossing voor antibioticaresistentie
Nanodeeltjes als mogelijke oplossing voor antibioticaresistentie Welk mineraal is hoogstwaarschijnlijk een ingrediënt dat wordt gebruikt in babypoeder?
Welk mineraal is hoogstwaarschijnlijk een ingrediënt dat wordt gebruikt in babypoeder?  Wat heeft elk klein beetje materie uitgeoefend de kracht van?
Wat heeft elk klein beetje materie uitgeoefend de kracht van?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


