
Wetenschap
Is OCL2 een moleculaire of ionische binding?
* Elektronegativiteitsverschil: Zuurstof is elektronegatiefer dan chloor. Hoewel er een verschil is in elektronegativiteit, is het niet groot genoeg om ionische bindingen te vormen. Het verschil in elektronegativiteit leidt tot polaire covalente bindingen .
* gedeelde elektronen: Zuurstof en chloor delen elektronen om covalente bindingen te vormen. Dit delen resulteert in de vorming van een molecuul.
* Algemeen lading: OCL2 is een neutraal molecuul. Er is geen netto positieve of negatieve lading. Ionische verbindingen hebben daarentegen een kation (positief ion) en een anion (negatief ion).
Samenvattend: OCL2 vormt een moleculaire structuur als gevolg van het delen van elektronen tussen zuurstof en chlooratomen door polaire covalente bindingen.
 Wat zijn de functies van de Cecum?
Wat zijn de functies van de Cecum?  Wereldwijd kankerrisico door verbranding van organisch materiaal komt van niet-gereguleerde chemicaliën
Wereldwijd kankerrisico door verbranding van organisch materiaal komt van niet-gereguleerde chemicaliën De niveaus van Tornadoes
De niveaus van Tornadoes Kenmerken van planten die het klimaat in de woestijn kunnen overleven
Kenmerken van planten die het klimaat in de woestijn kunnen overleven Satellietradargegevens onthullen krachtig smelten op de Thwaites-gletsjer op Antarctica
Satellietradargegevens onthullen krachtig smelten op de Thwaites-gletsjer op Antarctica
Hoofdlijnen
- Welke rol speelde Xray -foto van DNA in de ontdekkingsstructuur?
- Welke segmenten van DNA overgedragen van ouder op nakomelingen worden genoemd?
- Welke organen vormen het urogenitale systeem?
- Kunnen taalmodellen het genoom lezen? Deze decodeerde mRNA om betere vaccins te maken
- Een win-win voor gevlekte uilen en bosbeheer
- Gebruik van micro-organismen om grote ziekten te bestrijden die de rundvleesindustrie treffen
- Wat zijn de veranderingen in DNA -sequenties die invloed hebben op genetische informatie die bekend staat als?
- Wie is de oprichter en mede-oprichter van Theory Natural Selectie?
- Hoe noem je een groep organen die samenwerken om een belangrijke functie uit te voeren?
- Wat bacteriën ons kunnen leren over het bestrijden van atrazinebesmetting
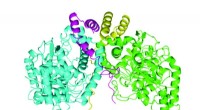
- (Re)generatie volgende:nieuwe strategie om steigers te ontwikkelen voor regeneratie van gewrichtsweefsel

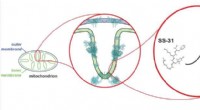
- Onderzoekers onderzoeken mogelijke behandeling voor mitochondriale ziekten
- Een olievlek opruimen

- Onderzoek onthult meer over het pad dat bacteriële ziekteverwekkers afleggen om tuberculose te veroorzaken

 Satellieten laten zien dat een ‘mega-ijsberg’ 152 miljard ton zoet water in de oceaan heeft geloosd toen deze langs Zuid-Georgië schraapte
Satellieten laten zien dat een ‘mega-ijsberg’ 152 miljard ton zoet water in de oceaan heeft geloosd toen deze langs Zuid-Georgië schraapte  Magische Sprong, het opstarten van 3D-software van 2 miljard dollar, is eindelijk live. Het komt niet goedkoop.
Magische Sprong, het opstarten van 3D-software van 2 miljard dollar, is eindelijk live. Het komt niet goedkoop. Wat voor soort kracht oefent u op waar op bed ligt?
Wat voor soort kracht oefent u op waar op bed ligt?  Zou de matrixmechanica vandaag de dag erkenning krijgen?
Zou de matrixmechanica vandaag de dag erkenning krijgen?  Snelle screening op potentiële nieuwe katalysatoren
Snelle screening op potentiële nieuwe katalysatoren Hoe werken Golgi-lichamen om celproducten op te slaan?
Hoe werken Golgi-lichamen om celproducten op te slaan?  Hoe wordt ruwe olie naar het aardoppervlak gebracht?
Hoe wordt ruwe olie naar het aardoppervlak gebracht?  Hoe is de efficiëntie afhankelijk van massa en waarom is het zo?
Hoe is de efficiëntie afhankelijk van massa en waarom is het zo?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

