
Wetenschap
Is overtollig natriumhydroxide oplosbaar in water?
Dit is waarom:
* NaOH is een sterke basis: Het dissocieert gemakkelijk in water en vormt natriumionen (Na+) en hydroxide-ionen (OH-).
* Oplosbaarheid neemt toe met temperatuur: Hoewel NaOH bij kamertemperatuur zeer oplosbaar is, neemt de oplosbaarheid aanzienlijk toe naarmate de watertemperatuur stijgt.
Er zijn echter enkele praktische beperkingen:
* Verzadigingspunt: Hoewel NaOH zeer oplosbaar is, is er een limiet aan hoeveel kan oplossen in een bepaalde hoeveelheid water bij een specifieke temperatuur. Dit staat bekend als het verzadigingspunt. Afgezien van dit punt zal elke extra NaOH niet oplossen.
* exotherme reactie: Het oplossen van NaOH in water is een exotherme reactie, wat betekent dat het warmte vrijgeeft. Als u te veel NaOH toevoegt, kan de oplossing erg heet worden en mogelijk gevaren veroorzaken.
Daarom is het, hoewel overtollige NaOH in water kan worden opgelost, het belangrijk om het verzadigingspunt en de veiligheidsmaatregelen te overwegen bij het hanteren van grote hoeveelheden.
Hoofdlijnen
- Hoe komt het dat uw planeet niet bedekt is met bacteriën?
- Nieuwe modellen stellen oude aannames in vraag over hoeveel moleculen er nodig zijn om de celdeling te controleren
- Gebruiken paddenstoelen echt taal om met elkaar te praten? Een schimmelexpert onderzoekt
- Wetenschappers ontdekken hoe sommige bacteriën antibiotica overleven
- Hoe wordt een wetenschappelijke hypothese gevormd?
- Welke genen maakt geen deel uit van het lac -operon?
- Mysteriegen rijpt het skelet van de cel
- Wat is een ander woord dat wetenschappers fouten gebruiken?
- Studie onderzoekt biologie, impact, beheer en potentiële verspreiding van destructieve boktor
- Wetenschappers hebben nieuwe manier gevonden om chirale tetraarylmethaan te synthetiseren
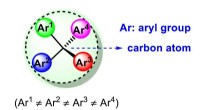
- Goedkopere waterstofbrandstofcel kan betere groene energie-opties betekenen

- Gepersonaliseerde zweetsensor meet betrouwbaar de bloedglucose zonder vingerprikken

- Onderzoekers ontwikkelen zelfaangedreven microfluïdische plaat die zich wikkelt, flappen en kruipen
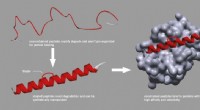
- Nieuwe aanpak om peptidestapeling algemeen beschikbaar te maken
 Wat is de relatie tussen klimaat en landbouw?
Wat is de relatie tussen klimaat en landbouw?  Onderzoeksteam bestudeert geologie van bosbranden
Onderzoeksteam bestudeert geologie van bosbranden Vijf massale uitstervingen - en wat we ervan kunnen leren over de planeet vandaag
Vijf massale uitstervingen - en wat we ervan kunnen leren over de planeet vandaag Joe duwt op een doos van 14 kg met een kracht van 130 N Toch de enige bewegingen met 3 meter per seconde kwadrated Wat is de grootteweerstand in Newtons?
Joe duwt op een doos van 14 kg met een kracht van 130 N Toch de enige bewegingen met 3 meter per seconde kwadrated Wat is de grootteweerstand in Newtons?  Een rubberen computer elimineert de laatste harde componenten van zachte robots
Een rubberen computer elimineert de laatste harde componenten van zachte robots Hoe lang kan een persoon veilig ondersteboven hangen?
Hoe lang kan een persoon veilig ondersteboven hangen?  Wat is het exosfeer te boven?
Wat is het exosfeer te boven?  Een bevolkingsdichtheid berekenen
Een bevolkingsdichtheid berekenen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


