
Wetenschap
Wat is het atoomnummer n?
Dit is wat je moet weten:
* Atomisch nummer: Dit is het aantal protonen in de kern van een atoom. Het definieert welk element het atoom is (bijv. Koolstof heeft atoomnummer 6).
* Hoofdkwantumnummer (n): Dit beschrijft het energieniveau van het elektron. Het is een positief geheel getal (n =1, 2, 3, ...) met hogere getallen die een hogere energieniveaus aangeven.
Sleutelpunten:
* n =1: Vertegenwoordigt het laagste energieniveau, ook wel de grondtoestand genoemd.
* n =2, 3, enz.: Vertegenwoordigen hogere energieniveaus, geëxciteerde toestanden genoemd.
* elektronen kunnen tussen energieniveaus springen: Dit gebeurt wanneer een atoom licht absorbeert of uitzendt (fotonen).
Voorbeeld:
In een waterstofatoom bevindt het elektron zich meestal in de n =1 toestand (grondtoestand). Als het energie absorbeert, kan het naar de n =2 -toestand springen (opgewonden toestand).
Laat het me weten als je meer vragen hebt!
 Nieuwe stabiele isotopenanalyse stelt de oorsprong van zwarte koolstof in de oceaan in vraag
Nieuwe stabiele isotopenanalyse stelt de oorsprong van zwarte koolstof in de oceaan in vraag Beschrijf de soorten fossielen
Beschrijf de soorten fossielen Duurzaam winkelen - haal het zwerfvuil uit glitter
Duurzaam winkelen - haal het zwerfvuil uit glitter Online platform om de paraatheid bij rampen te verbeteren met behulp van gemeenschapsgegevens, het in kaart brengen van hulpbronnen en AI
Online platform om de paraatheid bij rampen te verbeteren met behulp van gemeenschapsgegevens, het in kaart brengen van hulpbronnen en AI  Radarbeelden laten zien dat een groot deel van het olieveld in Texas met alarmerende snelheden deinende en zinkt
Radarbeelden laten zien dat een groot deel van het olieveld in Texas met alarmerende snelheden deinende en zinkt
Hoofdlijnen
- Verschillen tussen "Fysiek" en "Fysiologisch"
- Wat zijn de verschillende vormen van wetenschappelijke kennis?
- Wat is de overdracht van mannelijke pollenkorrel naar vrouwelijk orgaan?
- Hoe heet Human Herpesvirus 8 ook?
- Wat gebeurt er met het anaërobe organisme in aanwezigheid van zuurstof?
- Wat is een eenvoudige bacterie?
- Is een steroïde eiwit lipide koolhydraat of nucleïnezuur?
- De richting van synthese is een RNA -transcript?
- Iberische bruine beren stammen niet af van degenen die tijdens de ijstijd uit het noorden zijn gevlucht
- Nieuw zuurvrij magneetrecyclingproces

- Nieuwe 2D-spectroscopiemethoden

- Bekledingstests tonen aan dat vocht de Grenfell-vlammen mogelijk heeft versneld

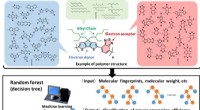
- AI-software helpt bij het ontwerpen van nieuw materiaal voor zonnecellen
- Nieuwe composietmaterialen verlengen de levensduur van reserveonderdelen voor apparatuur en voertuigen

 Sneeuw boven Antarctica bufferde zeespiegelstijging vorige eeuw
Sneeuw boven Antarctica bufferde zeespiegelstijging vorige eeuw Eerste willekeurige laser gemaakt van keramiek op papierbasis
Eerste willekeurige laser gemaakt van keramiek op papierbasis Satellietgegevens tonen verlies van sneeuwbedekking, niet roet verantwoordelijk voor snelle temperatuurstijging in het noordpoolgebied
Satellietgegevens tonen verlies van sneeuwbedekking, niet roet verantwoordelijk voor snelle temperatuurstijging in het noordpoolgebied Waar kunt u zien dat Gassess is gebruikt, worden geproduceerd, schrijf uw bevinding in een tabel?
Waar kunt u zien dat Gassess is gebruikt, worden geproduceerd, schrijf uw bevinding in een tabel?  Batterijen zoals ze bedoeld zijn om gezien te worden
Batterijen zoals ze bedoeld zijn om gezien te worden Hoe gebruiken geografen kompassen?
Hoe gebruiken geografen kompassen?  Garnalenklauw inspireert nieuwe methode voor het genereren van plasma onder water
Garnalenklauw inspireert nieuwe methode voor het genereren van plasma onder water Vulkaaninformatie voor kinderen
Vulkaaninformatie voor kinderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

