
Wetenschap
Wat is de oxidatietoestand van waterstof in peroxide?
De oxidatietoestand van waterstof in waterstofperoxide (H₂o₂) is +1 .
Dit is waarom:
* zuurstof is meer elektronegatief dan waterstof. Dit betekent dat zuurstof een sterkere trek heeft op de gedeelde elektronen in de H-O-binding.
* zuurstof heeft meestal een oxidatietoestand van -2 In de meeste verbindingen, behalve in peroxiden.
* In waterstofperoxide heeft elk zuurstofatoom een oxidatietoestand van -1 . Dit komt omdat de twee zuurstofatomen aan elkaar worden gebonden en de elektronen in die binding gelijk worden gedeeld.
* om de kosten in evenwicht te brengen , elk waterstofatoom moet een oxidatietoestand van +1 hebben.
Daarom is de algehele oxidatietoestand van waterstofperoxide:
2 (+1) + 2 (-1) =0
 Wat is precies het tegenovergestelde van ionisatie?
Wat is precies het tegenovergestelde van ionisatie?  Wat is het voordeel van covalente binding ten opzichte van ionische binding bij het maken van grote moleculen?
Wat is het voordeel van covalente binding ten opzichte van ionische binding bij het maken van grote moleculen?  Welk metaal kan natrium verplaatsen?
Welk metaal kan natrium verplaatsen?  Wat zijn de belangrijkste zeezouten?
Wat zijn de belangrijkste zeezouten?  Zullen sterke en snel wisselende kunstmatige spieren haalbaar zijn?
Zullen sterke en snel wisselende kunstmatige spieren haalbaar zijn?
 Irak koestert amberkleurige rijstoogst verwoest door droogte
Irak koestert amberkleurige rijstoogst verwoest door droogte Uw rit koolstofarm maken voor een stabieler klimaat
Uw rit koolstofarm maken voor een stabieler klimaat OMG, de wateren warm! NASA-studie lost gletsjerpuzzel op
OMG, de wateren warm! NASA-studie lost gletsjerpuzzel op UMD en Resilinc Corp. creëren index van risico op klimaatverandering voor toeleveringsketens van bedrijven
UMD en Resilinc Corp. creëren index van risico op klimaatverandering voor toeleveringsketens van bedrijven De VS zegt dat twee forever-chemicaliën gevaarlijk zijn en zegt tegen de vervuilers dat ze moeten betalen
De VS zegt dat twee forever-chemicaliën gevaarlijk zijn en zegt tegen de vervuilers dat ze moeten betalen
Hoofdlijnen
- Wat maakt je een wetenschapper?
- Een persoon die wetenschap studeert?
- Grizzlies vertonen opmerkelijke gencontrole vóór en tijdens de winterslaap
- Hoe coördineren cellen hun gedrag met anderen om gedrag op weefselschaal te creëren?
- In welk type cellen resulteert mitose?
- Hoe ondersteunen fossiele en biochemicaliën de evolutietheorie?
- Welke cytoskeletale eiwitten zijn belangrijke bestanddelen van de contractiele structuren die splitsing vormen die betrokken zijn bij cytokinese van diercellen?
- Wat is een persoon die bestudeert hoe insecten worden genoemd en gegroepeerd?
- Wat zijn aanpassingen van cyanobacteriën?
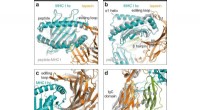
- Moleculaire chaperonne-interacties gevisualiseerd door middel van röntgenstructuuranalyse
- Er gebeuren vreemde dingen als een kristal in tweeën wordt gesplitst

- Nieuw materiaal kan giftige stoffen uit de lucht opvangen

- Onderzoekers werpen nieuw licht op mysteries achter de lichtemissie van vuurvliegjes

- Massaproductie van geïndividualiseerde producten

 Hoe werken cellen samen om een persoon te vormen?
Hoe werken cellen samen om een persoon te vormen?  Wat is een drone?
Wat is een drone?  Onderzoekers observeren continu tijdkristal
Onderzoekers observeren continu tijdkristal Produceert elektromagnet elektriciteit of gebruikt u elektriciteit?
Produceert elektromagnet elektriciteit of gebruikt u elektriciteit?  In welke reeks fasen zie je minder de maan?
In welke reeks fasen zie je minder de maan?  Onderzoek naar platentektoniek herschrijft de geschiedenis van de continenten van de aarde
Onderzoek naar platentektoniek herschrijft de geschiedenis van de continenten van de aarde Hoeveel momentum heeft een object dat niet beweegt?
Hoeveel momentum heeft een object dat niet beweegt?  Hoeveel oz is 180 gram?
Hoeveel oz is 180 gram?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

