
Wetenschap
Wat combineert gemakkelijk met waterstofionen?
Hier is een uitsplitsing:
* bases Bevat hydroxide-ionen (OH-), die gemakkelijk reageren met waterstofionen om water te vormen. Dit is de fundamentele basis van zuur-base neutralisatie.
* Alkalische stoffen zijn vergelijkbaar met basen, maar bevatten mogelijk geen hydroxide -ionen. Ze kunnen nog steeds reageren met waterstofionen om water en zout te produceren.
Voorbeeld:
* zoutzuur (HCl) is een sterk zuur, wat betekent dat het gemakkelijk waterstofionen vrijgeeft. Wanneer het reageert met natriumhydroxide (NaOH) , een sterke basis, het vormt water (H2O) en natriumchloride (NaCl) - zout :
`` `
HCl (aq) + NaOH (aq) → h2o (l) + NaCl (aq)
`` `
Samenvattend:
* Bases en alkalische stoffen zijn de meest voorkomende stoffen die gemakkelijk combineren met waterstofionen.
* Deze reactie is een fundamenteel concept in de chemie die bekend staat als zure-base neutralisatie .
* Het product van deze reactie is altijd water en een zout .
 Elke verbinding die het aantal hydroxide -ionen verhoogt wanneer opgelost in waterbases rood litmus papier blauw worden en reageren met zuren om zout te vormen?
Elke verbinding die het aantal hydroxide -ionen verhoogt wanneer opgelost in waterbases rood litmus papier blauw worden en reageren met zuren om zout te vormen?  5de rang Chemieversleuteld activiteit
5de rang Chemieversleuteld activiteit Naam 6 Methoden voor het scheiden van materialen?
Naam 6 Methoden voor het scheiden van materialen?  Hoeveel alfa-emissies zouden Francium-223 converteren naar Bismuth-215?
Hoeveel alfa-emissies zouden Francium-223 converteren naar Bismuth-215?  Wat is een ozon -gootsteen?
Wat is een ozon -gootsteen?
 Hoe een over het hoofd gezien onderzoek van meer dan een eeuw geleden de Colorado River-crisis heeft aangewakkerd
Hoe een over het hoofd gezien onderzoek van meer dan een eeuw geleden de Colorado River-crisis heeft aangewakkerd  Steenkool is nog steeds de koning in de wereldwijde elektriciteitsproductie
Steenkool is nog steeds de koning in de wereldwijde elektriciteitsproductie Race om mensen te redden die zijn gestrand in Amerikaanse orkaan
Race om mensen te redden die zijn gestrand in Amerikaanse orkaan Afbeelding:Lima, Peru gezien vanuit een baan om de aarde
Afbeelding:Lima, Peru gezien vanuit een baan om de aarde Planten die testosteron bevatten
Planten die testosteron bevatten
Hoofdlijnen
- Nieuwe celvrije eiwitkristallisatiemethode om structurele biologie te bevorderen
- Waar komt fotosynthese voor in planten- en algencellen?
- Eenheid van inherent in dat wordt doorgegeven van ouder tot nakomelingen?
- De 3 regels voor het benoemen van organismen waren?
- Wat is een wetenschappelijk woord voor de grootste?
- Hoe is ATP -synthase betrokken bij het maken van energie van de cel?
- Wat is een voorbeeld van biologische hypothese?
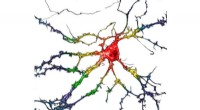
- Hoe functioneert een zenuwcelfunctie bij de mens?
- Wat is de genetische samenstelling van een organisme?
- Moleculaire trillingen benutten om geleidende polymeren te synthetiseren

- Nieuwe theorie over kruisverschijnselen kan de effectiviteit van nieuwe materialen voorspellen

- De vorm van zachte materie veranderen met behulp van logische circuits gemaakt van DNA
- Onderzoekers identificeren een psychedelisch-achtig medicijn zonder de hallucinogene bijwerkingen
- Wetenschappers coderen Wizard of Oz in een verdwijnend klein plastic

 Zitten toeleveringsketens vast in detentie?
Zitten toeleveringsketens vast in detentie? Welk materiaal heeft een slechte energiegeleider?
Welk materiaal heeft een slechte energiegeleider?  Zijn er ringen in een baan om Mars of is hoe ze eruit zien en wanneer zijn ontdekt?
Zijn er ringen in een baan om Mars of is hoe ze eruit zien en wanneer zijn ontdekt?  Silicium nanodeeltjes effenen de weg naar lichtemitters op nanoschaal
Silicium nanodeeltjes effenen de weg naar lichtemitters op nanoschaal Wie heeft de ontdekking gedaan die de elektromagnetische lichttheorie vond?
Wie heeft de ontdekking gedaan die de elektromagnetische lichttheorie vond?  Welke energie biedt vet?
Welke energie biedt vet?  Kun je een glas met een hoge noot echt verbrijzelen?
Kun je een glas met een hoge noot echt verbrijzelen?  Hoe is het mogelijk dat een raket zich door de ruimte voortstuwt?
Hoe is het mogelijk dat een raket zich door de ruimte voortstuwt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

