
Wetenschap
Bariumchloride en natriumsulfaat in water reageren om onoplosbaar barium de oplossing van chloride te geven?
De reactie:
Bariumchloride (BACL₂) en natriumsulfaat (Na₂so₄) reageren in een waterige oplossing om onoplosbaar bariumsulfaat (baso₄) te vormen en oplosbaar natriumchloride (NaCl) .
De vergelijking:
Bacl₂ (aq) + na₂so₄ (aq) → baso₄ (s) + 2nacl (aq)
Verklaring:
* bariumsulfaat (baso₄) is een wit, vast neerslag dat praktisch onoplosbaar is in water. Daarom vormt het een vaste stof in de reactie.
* natriumchloride (NaCl) , ook bekend als tafelzout, is zeer oplosbaar in water en blijft opgelost in de oplossing.
Sleutelpunten:
* Oplosbaarheid: De reactie hangt af van de oplosbaarheidsregels van ionische verbindingen. Sommige zouten zijn oplosbaar, terwijl anderen dat niet zijn.
* neerslag: De vorming van het onoplosbare bariumsulfaat (Baso₄) is de drijvende kracht achter de reactie. Het neerslag scheidt van de oplossing.
Laat het me weten als je nog meer vragen hebt!
 Welke elementen Noble-GAS-configuratie bevat XE?
Welke elementen Noble-GAS-configuratie bevat XE?  Heeft Scott Pruitt goede argumenten voor het intrekken van de Clean Water Rule?
Heeft Scott Pruitt goede argumenten voor het intrekken van de Clean Water Rule?  Wat is een goed oplosmiddel voor herkristallisatie van natriumbenzoaat?
Wat is een goed oplosmiddel voor herkristallisatie van natriumbenzoaat?  Welke verbinding moet worden toegevoegd aan het verkrijgen van poeder om chloor te verkrijgen?
Welke verbinding moet worden toegevoegd aan het verkrijgen van poeder om chloor te verkrijgen?  Laagste temperatuur waarbij een enzym kan werken?
Laagste temperatuur waarbij een enzym kan werken?
 Steden en landen streven ernaar om binnen tien jaar plastic afval te verminderen
Steden en landen streven ernaar om binnen tien jaar plastic afval te verminderen Nieuw onderzoek zet vraagtekens bij de snelheid van klimaatverandering
Nieuw onderzoek zet vraagtekens bij de snelheid van klimaatverandering Tropische regenwoudplanten voor kinderen
Tropische regenwoudplanten voor kinderen Eten vleermuizen muggen of motten? De aanwijzing zit in de poep
Eten vleermuizen muggen of motten? De aanwijzing zit in de poep  Doritos, eendjes en onstoffelijke voeten:hoe tragedie en geluk de verborgen snelwegen van de oceanen onthullen
Doritos, eendjes en onstoffelijke voeten:hoe tragedie en geluk de verborgen snelwegen van de oceanen onthullen
Hoofdlijnen
- Welk proces produceert klonen?
- Een nieuwe rol voor de eiwitfamilie zou een pad kunnen bieden voor de manier waarop gewaseigenschappen worden gewijzigd
- Een biohybride robot gemaakt van meel en haver zou kunnen fungeren als een biologisch afbreekbare vector voor herbebossing
- Chemici laten zien dat de natuur verschillende eiwitbouwstenen had kunnen gebruiken
- Onderzoek onthult de sleutelrol van de communicatie tussen planten en bacteriën bij de assemblage van een gezond plantenmicrobioom
- Chargaff -bijdrage aan de structuur van DNA?
- Hoe identificeer je de water die cellen draagt in een stengel van selderij?
- Is algenvernietigerzuur of basis?
- Wat zijn de verschillen tussen bacteriecellen en plantencellen?
- Licht pincet kan bewegen, smelten, en verstrooi mysterieuze biologische ijsbergen

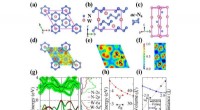
- Machine learning voorspelde een superhard wolfraamnitride met hoge energiedichtheid
- De pH van calciumionen regelt de opening van het ionkanaal

- Nieuwe melkzuurbacteriën zorgen voor natuurlijke zoetheid in yoghurt

- Actie van geneesmiddelverbindingen in weefsel onthuld door nieuwe techniek
 Wat is de heetste planeet in zonne -sistem?
Wat is de heetste planeet in zonne -sistem?  Wat is waar aan deze zonne -energie die als warmte wordt geabsorbeerd en vrijgegeven door oppervlak?
Wat is waar aan deze zonne -energie die als warmte wordt geabsorbeerd en vrijgegeven door oppervlak?  Wat is het effect dat u kunt zien als er licht uit een deeltje stuitert?
Wat is het effect dat u kunt zien als er licht uit een deeltje stuitert?  Hoe verschillen isomeren van een alkeen als ze dezelfde moleculaire formules hebben?
Hoe verschillen isomeren van een alkeen als ze dezelfde moleculaire formules hebben?  Wat is het verschil tussen vormen en soorten energie?
Wat is het verschil tussen vormen en soorten energie?  Waar komt de zon op?
Waar komt de zon op?  Wat zijn de praktische toepassingen van Newtons Second Law Motion?
Wat zijn de praktische toepassingen van Newtons Second Law Motion?  Nieuw grafeen nanomesh kan de toekomst van elektronica veranderen
Nieuw grafeen nanomesh kan de toekomst van elektronica veranderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

