
Wetenschap
Waarom gesmolten koperchloride elektriciteit leiden?
Dit is waarom:
* ionische verbindingen: Koperchloride is een ionische verbinding, wat betekent dat deze wordt gevormd door de elektrostatische aantrekkingskracht tussen positief geladen koperionen (Cu²⁺) en negatief geladen chloride -ionen (CL⁻).
* vaste toestand: In zijn vaste toestand zijn de ionen strak verpakt in een kristalrooster, waardoor het een slechte geleider is. De ionen zijn in positie gefixeerd en kunnen niet vrij bewegen.
* gesmolten toestand: Wanneer koperchloride wordt gesmolten, worden de sterke elektrostatische krachten die de ionen bij elkaar houden, overwonnen. Hierdoor kunnen de ionen vrij in de vloeistof bewegen.
* elektrische stroom: Wanneer een elektrisch potentieel wordt toegepast over het gesmolten koperchloride, bewegen de positief geladen koperionen naar de negatieve elektrode (kathode) en bewegen de negatief geladen chloride -ionen naar de positieve elektrode (anode). Deze beweging van ionen vormt een elektrische stroom.
Daarom stelt de aanwezigheid van vrije, mobiele ionen in gesmolten koperchloride het in staat elektriciteit te leiden.
 Welk bewijs heb je dat het evenwicht verschoof toen de verzadigde kaliumnitraatoplossing werd afgekoeld?
Welk bewijs heb je dat het evenwicht verschoof toen de verzadigde kaliumnitraatoplossing werd afgekoeld?  Drie dingen die je waarneemt in een chemische verandering van mengsel Mg-Cuso4?
Drie dingen die je waarneemt in een chemische verandering van mengsel Mg-Cuso4?  Waarom is het smeltpunt van ammoniak lager dan water?
Waarom is het smeltpunt van ammoniak lager dan water?  Hoe kunt u de hardheid van mineraal bepalen?
Hoe kunt u de hardheid van mineraal bepalen?  Wat is zinkpoeder?
Wat is zinkpoeder?
 Hoe bossen in een paar generaties 8.000 jaar aan opgeslagen koolstof verloren
Hoe bossen in een paar generaties 8.000 jaar aan opgeslagen koolstof verloren Semeru-vulkaan op het Indonesische Java-eiland spuwt hete wolken
Semeru-vulkaan op het Indonesische Java-eiland spuwt hete wolken Is kleding een natuurlijke bodembron?
Is kleding een natuurlijke bodembron?  Wat kunt u zeggen over het bestaan en de diversiteit van het leven vóór de ozonlaag van de formatie?
Wat kunt u zeggen over het bestaan en de diversiteit van het leven vóór de ozonlaag van de formatie?  De koloniale geschiedenis van de Marshalleilanden beperkt hun vermogen om zichzelf te redden van klimaatverandering
De koloniale geschiedenis van de Marshalleilanden beperkt hun vermogen om zichzelf te redden van klimaatverandering
Hoofdlijnen
- Zou het hebben van een eigen kloon hetzelfde zijn als het hebben van een identieke tweeling?
- Hoe één soort uiteindelijk de dominante partner kan worden in een mutualistische relatie
- The Anatomy of the Hydra
- Wat is het belang van virtual reality voor artsen en chirurgen?
- Wat is correct met betrekking tot een sferische cel?
- Is de overbevissing voorbij? Een Amerikaanse topwetenschapper zegt ja
- Wat is een virus en hoe wordt het een gevaar voor het menselijk leven?
- Warmer watersignalen veranderen voor Schotse shags
- Onderzoekers bestuderen de complexiteit van homologe recombinatie en abnormale chromosoombruggen
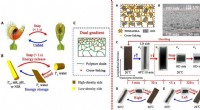
- Ontwikkeling van een ultrasnel biomimetisch snapping hydrogelmateriaal met twee gradiënten
- Zijn elementair:Ultra-sporendetector test de zuiverheid van goud

- Zou de aarde van gisteren aanwijzingen kunnen bevatten voor het maken van de medicijnen van morgen?

- Unboil een eiermachine zorgt voor een verbeterde bacteriedetector
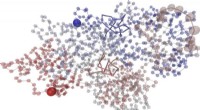
- Natuurkundigen gebruiken wiskundige algoritmen om experimentele 3D-structuren van chromosomen te onderzoeken
 Heterogene ethyleenhydroformylering maakt een zeer efficiënte industriële productie van propanal/n-propanol mogelijk
Heterogene ethyleenhydroformylering maakt een zeer efficiënte industriële productie van propanal/n-propanol mogelijk Maakt 3D-printen de hype waar?
Maakt 3D-printen de hype waar?  Wat is de moleculaire formule voor benzine?
Wat is de moleculaire formule voor benzine?  Het in Abu Dhabi gevestigde bureau roept op tot verdubbeling van investeringen in schone energie
Het in Abu Dhabi gevestigde bureau roept op tot verdubbeling van investeringen in schone energie Hoe wordt een astronomische eenheid gedefinieerd?
Hoe wordt een astronomische eenheid gedefinieerd?  Welke straling wordt uitgegeven wanneer een positron botst met een elektron?
Welke straling wordt uitgegeven wanneer een positron botst met een elektron?  Hoe kun je een relatieve vochtigheid gebruiken?
Hoe kun je een relatieve vochtigheid gebruiken?  Wordt de snelheid van de bal tijdens de hele vlucht of op bepaalde momenten veranderd?
Wordt de snelheid van de bal tijdens de hele vlucht of op bepaalde momenten veranderd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

