
Wetenschap
Wat zou het grootste volume van 0,100 m natriumhydroxide -oplossing vereisen voor neutralisatie?
* De identiteit van het zuur: Verschillende zuren hebben verschillende aantallen zure protonen (H+ -ionen) die kunnen worden geneutraliseerd door NaOH.
* De concentratie van het zuur: Een hogere zuurconcentratie vereist meer NaOH voor neutralisatie.
* Het volume van het zuur: Een groter volume zuur vereist meer NaOH voor neutralisatie.
Hier is hoe je erover nadenkt:
* Neutralisatiereactie: De reactie tussen een zuur en een basis (zoals NaOH) omvat de reactie van H+ -ionen uit het zuur met OH-ionen van de basis om water te vormen.
* mol: Om een zuur volledig te neutraliseren, heb je een gelijk aantal mol H+ ionen en oh-ionen nodig.
* Volume en concentratie: Het aantal mol een stof wordt berekend door zijn concentratie (molariteit) te vermenigvuldigen met zijn volume (in liters).
Voorbeeld:
Laten we zeggen dat we twee zuren hebben, a en b:
* zuur A: 0,200 m HCl (zoutzuur) - heeft één zuur proton per molecuul
* zuur B: 0,100 m H2SO4 (zwavelzuur) - heeft twee zure protonen per molecuul
Om hetzelfde volume van elk zuur te neutraliseren, zouden we nodig hebben:
* zuur A: 1 mol NaOH per mol HCl
* zuur B: 2 mol NaOH per mol H2SO4 (omdat het twee zure protonen heeft)
Daarom zou een hogere concentratie zuur of zuur met meer zure protonen een groter volume van 0,100 m NaOH vereisen voor neutralisatie.
Om u een definitief antwoord te geven, geeft u de volgende informatie op:
* De identiteit van het zuur (en) dat u vergelijkt
* De concentratie van elk zuur
* Het volume van elk zuur (indien van toepassing)
 Critici van Green New Deal zien door de bomen het bos niet meer
Critici van Green New Deal zien door de bomen het bos niet meer Verhoogt het bos bodemerosie?
Verhoogt het bos bodemerosie?  Ten minste 2% van de openbare watersystemen in de VS zijn als Flints - Amerikanen horen er gewoon niets over
Ten minste 2% van de openbare watersystemen in de VS zijn als Flints - Amerikanen horen er gewoon niets over Onderzoekers ontdekken bewijs van aardbevingen die de Chileense kust in de afgelopen 9 hebben getroffen 000 jaar
Onderzoekers ontdekken bewijs van aardbevingen die de Chileense kust in de afgelopen 9 hebben getroffen 000 jaar Microplastics kunnen de snelheid waarmee koolstof van het zeeoppervlak naar de diepte wordt getrokken vertragen
Microplastics kunnen de snelheid waarmee koolstof van het zeeoppervlak naar de diepte wordt getrokken vertragen
Hoofdlijnen
- Nieuw soort cognitieve robot... een puppy?
- Wanneer een chromosoom op zichzelf in karyotype verschijnt en niet als paar staat het bekend als?
- Wil je een bluebottle-steek vermijden? Zo kun je voorspellen op welk strand ze zullen landen
- Wat zit er in een naam? Een glimp van de evolutie, het benoemen van baby's, het kiezen van een hond, studievondsten
- De reden voor incubatie bij verschillende temperaturen in de microbiologie
- Heeft Eubacteriën de aanwezigheid van complexe orgaansystemen?
- Kunnen darmbacteriën die ons helpen bij het verteren van bier en brood ook ziektes bestrijden?
- Hoe noem je een dier dat zowel nachtduur als dagelijkse is?
- Wat is de definitie van wetenschap voor kinderen?
- Wetenschappers onderzoeken macrocyclische peptiden als nieuwe medicijnsjablonen

- Waardoor ontstaat die piek? Een al lang bestaande vraag over covalente vloeistoffen beantwoorden
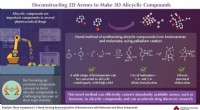
- Nieuwe methode kan op efficiënte wijze verschillende bouwstenen van farmaceutische medicijnen creëren
- Hoe melk een dierlijk lichaam goed doet?

- Nieuw apparaat kan warmte-energie omzetten in een levensvatbare brandstofbron
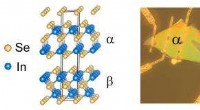
 Onderzoek toont aan dat autonome voertuigen de verkeersstroom kunnen helpen verbeteren
Onderzoek toont aan dat autonome voertuigen de verkeersstroom kunnen helpen verbeteren Waarom schijnt de zon niet overal?
Waarom schijnt de zon niet overal?  Waarom worden fluorchloorbroom en jodium in dezelfde groep geplaatst?
Waarom worden fluorchloorbroom en jodium in dezelfde groep geplaatst?  Waarom leven mossen in droog klimaat, zelfs als de grond water geeft?
Waarom leven mossen in droog klimaat, zelfs als de grond water geeft?  Unieke moleculaire CODE:paramagnetische codering van moleculen
Unieke moleculaire CODE:paramagnetische codering van moleculen Nanodeeltjes verbeteren de elektroden van lithiumbatterijen
Nanodeeltjes verbeteren de elektroden van lithiumbatterijen Welke materialen zou de beste isolator zijn voor een elektrische draad?
Welke materialen zou de beste isolator zijn voor een elektrische draad?  Atmosferische waarnemingen in China laten een stijging zien van de uitstoot van een krachtig broeikasgas
Atmosferische waarnemingen in China laten een stijging zien van de uitstoot van een krachtig broeikasgas
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

