
Wetenschap
Hoeveel eenzame paar elektronen bestaan er op het centrale atoom in ammoniak NH3?
Er is één Alleen al elektronen op het centrale stikstofatoom in ammoniak (NH3).
Dit is waarom:
* Valentie -elektronen van stikstof: Stikstof heeft 5 valentie -elektronen.
* Valentie -elektronen van waterstof: Elk waterstofatoom heeft 1 valentie -elektron.
* Totale valentie -elektronen: 5 (n) + 3 (h) =8 valentie -elektronen.
* binding: Stikstof vormt drie enkele bindingen met de drie waterstofatomen, met behulp van 6 valentie -elektronen.
* eenzaam paar: Dit laat 2 valentie -elektronen op het stikstofatoom, die een eenzaam paar vormen.
U kunt dit visualiseren met een Lewis -structuur:
H
|
H - n - h
|
H
De twee stippen op de stikstof vertegenwoordigen het enige paar.
 Verbeteren van de samenstelling van stralingsbeschermingsbrillen
Verbeteren van de samenstelling van stralingsbeschermingsbrillen Wat is de zuurdissociatieconstante voor een bij evenwicht HX is gelijk aan H positief) plus X (negatief)?
Wat is de zuurdissociatieconstante voor een bij evenwicht HX is gelijk aan H positief) plus X (negatief)?  Welke twee atomen vormen stikstof?
Welke twee atomen vormen stikstof?  Dallas Celanese en Under Armour werken samen aan een milieuvriendelijk spandexalternatief
Dallas Celanese en Under Armour werken samen aan een milieuvriendelijk spandexalternatief  Hoe de petro uit de petrochemische industrie te halen?
Hoe de petro uit de petrochemische industrie te halen?
 NASA volgt het doorweekte pad van Hanna naar Mexico
NASA volgt het doorweekte pad van Hanna naar Mexico Orkaan Fiona trekt richting Bermuda, VS adviseert burgers om reizen uit te stellen
Orkaan Fiona trekt richting Bermuda, VS adviseert burgers om reizen uit te stellen Bosranden zijn mogelijk beter bestand tegen klimaatverandering dan eerder werd gedacht
Bosranden zijn mogelijk beter bestand tegen klimaatverandering dan eerder werd gedacht Opwarmende vijvers kunnen klimaatverandering versnellen
Opwarmende vijvers kunnen klimaatverandering versnellen 5 landbouwtechnologieën die de wereld hebben veranderd
5 landbouwtechnologieën die de wereld hebben veranderd
Hoofdlijnen
- Wat is het kleine deel van de kern waar ribosomale subeenheid formatie plaatsvindt?
- Onderdrukt federaal rapport laat zien hoe het waterplan van Trump de Californische zalm in gevaar zou brengen
- Nieuwe methode bevordert de detectie van kanker door kleine bloedcirculerende deeltjes te tellen
- Heeft het menselijk haar invloed op de groei van planten?
- Warmer watersignalen veranderen voor Schotse shags
- Als een blad gefossiliseerd is, zou dit waarschijnlijk wat voor soort fossiel vormen?
- Wat is verantwoordelijk voor het ondersteunen van structor en beweging in cellen?
- Waarom zijn bacteriën het meest zorgwekkend?
- Onderzoek toont aan hoe externe ecologische gemeenschappen de co-evolutie van gastheren en hun parasieten kunnen beïnvloeden
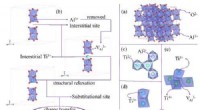
- Onderzoekers ontdekken de oorsprong van bijna-ultraviolette en zichtbare absorptiekenmerken van Ti:saffierlaserkristallen
- Triangle 2 plastic containers kunnen een make-over voor het milieu ondergaan
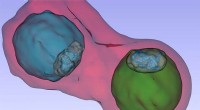
- Waterafstotend materiaal werpt af als een slang bij beschadiging

- Onderzoek naar perovskiet-silicium tandemcellen laat nieuwe weg zien

- Malariapathogeen onder de röntgenmicroscoop
 Wat waren de sociale economische en milieueffecten van 79 ad -uitbarsting Mount Vesuvius?
Wat waren de sociale economische en milieueffecten van 79 ad -uitbarsting Mount Vesuvius?  Hoeveel kubieke centimeter is een 6,2 liter?
Hoeveel kubieke centimeter is een 6,2 liter?  Wat meet satellietbeelden?
Wat meet satellietbeelden?  Jakob van Zyl, key Jet Propulsion Laboratory engineer, overlijdt
Jakob van Zyl, key Jet Propulsion Laboratory engineer, overlijdt Wat is het genotype van twee zwarte heterozygote cavia?
Wat is het genotype van twee zwarte heterozygote cavia?  Welk getij komt overeen met een zonsverduistering?
Welk getij komt overeen met een zonsverduistering?  Welke verandering zou optreden als de rotatie van de aarde aanzienlijk zou afnemen?
Welke verandering zou optreden als de rotatie van de aarde aanzienlijk zou afnemen?  Is behoud een goede of slechte zaak?
Is behoud een goede of slechte zaak?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

