
Wetenschap
Wat is de vergelijking voor de reactie van steenkool met zuurstof?
1. Volledige verbranding:
Dit is het ideale scenario waarbij steenkool volledig brandt en koolstofdioxide en water produceert.
* c (s) + o2 (g) → CO2 (g) + warmte
Deze vergelijking vertegenwoordigt de verbranding van zuivere koolstof, een belangrijk onderdeel van steenkool.
2. Onvolledige verbranding:
Dit gebeurt wanneer er niet genoeg zuurstof beschikbaar is voor volledige verbranding. Het kan koolmonoxide produceren, een giftig gas, samen met koolstofdioxide.
* 2c (s) + o2 (g) → 2co (g) + warmte
3. Real-world reacties:
In werkelijkheid is steenkool een complex mengsel van koolstof, waterstof, zwavel, stikstof en andere elementen. De werkelijke reactie is complexer en omvat meerdere stappen, waardoor verschillende bijproducten naast kooldioxide en water worden geproduceerd. Bijvoorbeeld:
* c (s) + h2o (g) → co (g) + h2 (g)
* c (s) + 2s (s) → Cs2 (g)
* c (s) + n2 (g) → 2cn (g)
factoren die de reactie beïnvloeden:
* Type kolen: Verschillende soorten steenkool hebben verschillende samenstellingen, die de producten en energieafgifte beïnvloeden.
* Beschikbaarheid van zuurstof: Onvoldoende zuurstof leidt tot onvolledige verbranding en meer verontreinigende stoffen.
* Temperatuur: Hogere temperaturen geven de voorkeur aan volledige verbranding.
* Druk: Druk kan de reactiesnelheid en de samenstelling van producten beïnvloeden.
Belangrijke opmerking: De verbranding van steenkool is een belangrijke bron van luchtvervuiling, waardoor broeikasgassen zoals koolstofdioxide, zwaveldioxide en stikstofoxiden worden vrijgelaten. Het is essentieel om de impact van het milieu te overwegen bij het gebruik van kolen als brandstofbron.
 Wetenschappers simuleren het klimaat van Game of Thrones
Wetenschappers simuleren het klimaat van Game of Thrones Hoe spinnen paren
Hoe spinnen paren  Wat beschrijft het zuurstofgehalte terwijl de aarde in de loop van de tijd evolueerde?
Wat beschrijft het zuurstofgehalte terwijl de aarde in de loop van de tijd evolueerde?  Synthesestudie toont aan dat fytoplankton kan bloeien onder Arctisch zee-ijs
Synthesestudie toont aan dat fytoplankton kan bloeien onder Arctisch zee-ijs Zeebodemgegevens wijzen op wereldwijd vulkanisme na Chicxulub-meteooraanval
Zeebodemgegevens wijzen op wereldwijd vulkanisme na Chicxulub-meteooraanval
Hoofdlijnen
- Een reeks gevouwen membranen die materialen in de cel verplaatsen?
- Een biohybride robot gemaakt van meel en haver zou kunnen fungeren als een biologisch afbreekbare vector voor herbebossing
- Wat wordt bedoeld met een sterke sleutel in de wetenschap?
- DNA RNA en ATP bevatten functionele eenheden die bekend staan als wat?
- Welke organellen maken de cel beweeglijk?
- Habitatverlies is de grootste bedreiging voor Australische soorten
- Wat vereist collageen synthese?
- UV-licht: positieve en negatieve effecten
- Waar worden belastingscellen het meest voor gebruikt?
- De computationele methoden van onderzoekers maken de weg vrij voor de volgende generatie membraantechnologie voor waterzuivering

- De breuktaaiheid van het materiaal voor vliegtuigbouw wordt 1,5 keer verhoogd

- Innovatiepioniers scoren wereldprimeur voor duurzaam bouwen met grafeenbeton

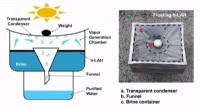
- Waterzuiveringssysteem op basis van hydrogel 12 keer beter dan huidige systemen
- Radicaal nieuw behandelingssysteem verlicht kankertherapie
 Als 0,500 mol van een niet-elektrolytische opgeloste stof wordt opgelost in 500,0 g ether, wat is dan de vriespuntoplossing?
Als 0,500 mol van een niet-elektrolytische opgeloste stof wordt opgelost in 500,0 g ether, wat is dan de vriespuntoplossing?  Wat is de atomaire massa van orthofosfairzuur?
Wat is de atomaire massa van orthofosfairzuur?  Hoe veroorzaakt de zwaartekracht erosie van het aardoppervlak?
Hoe veroorzaakt de zwaartekracht erosie van het aardoppervlak?  Sociale dilemma's begrijpen door middel van games - de ontwikkeling van morele normen moedigt onbaatzuchtig gedrag aan
Sociale dilemma's begrijpen door middel van games - de ontwikkeling van morele normen moedigt onbaatzuchtig gedrag aan  Waarom zou een bergachtig gebied met overvloedige regenval meestal meer rotsval hebben dan berg in een droog klimaat?
Waarom zou een bergachtig gebied met overvloedige regenval meestal meer rotsval hebben dan berg in een droog klimaat?  Die kaarten van het pad van de eclips? 'Fout', zeggen experts, met een afstand van wel een halve mijl aan de rand
Die kaarten van het pad van de eclips? 'Fout', zeggen experts, met een afstand van wel een halve mijl aan de rand  Wat was de naam van ruimtevaartuigen die voor het eerst op de maan landde?
Wat was de naam van ruimtevaartuigen die voor het eerst op de maan landde?  Wat doet oplosbaar in wetenschap?
Wat doet oplosbaar in wetenschap?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

