
Wetenschap
Hoe converteer je een neutrale zwavelatoom naar een anion met lading van -2?
Inzicht in de basis
* Neutrale zwavel: Een neutraal zwavelatoom heeft 16 protonen (positieve lading) en 16 elektronen (negatieve lading), wat resulteert in een netto lading van 0.
* anion: Een anion is een atoom of molecuul dat een of meer elektronen heeft opgedaan, waardoor het een negatieve lading heeft.
De conversie
1. Elektronenversterking: Zwavel moet twee elektronen krijgen om een -2 lading te bereiken. Dit komt omdat zwavel, net als alle atomen, ernaar streeft een stabiele elektronenconfiguratie te bereiken, zoals de edelgassen. Voor zwavel betekent dit dat 8 elektronen in de buitenste schaal hebben.
2. Elektronenconfiguratie:
* Neutrale zwavel (s):1S² 2S² 2P⁶ 3S² 3P⁴ (heeft 6 elektronen in de buitenste schaal)
* Sulfide -anion (S²⁻):1S² 2S² 2P⁶ 3S² 3P⁶ (heeft nu 8 elektronen in de buitenste schaal, zoals Argon)
Representatie
De conversie kan worden weergegeven door de volgende vergelijking:
S + 2e⁻ → S²⁻
Samenvattend
Om een neutrale zwavelatoom om te zetten in een sulfide -anion (S²⁻), moeten twee elektronen worden toegevoegd aan de elektronenwolk. Dit proces resulteert in een stabiele elektronenconfiguratie en een -2 lading op het zwavelatoom.
 Hoeveel mol Co² geproduceerd door de reactie 2.0 ch⁴ met overtollige o²?
Hoeveel mol Co² geproduceerd door de reactie 2.0 ch⁴ met overtollige o²?  Wat reinigt een cent beter dennen-sol of ontsmettingsalcohol dit is een wetenschapsproject?
Wat reinigt een cent beter dennen-sol of ontsmettingsalcohol dit is een wetenschapsproject?  Wat zijn de chemische eigenschappen van groep 8 -elementen?
Wat zijn de chemische eigenschappen van groep 8 -elementen?  Wat zijn externe toezichthouders?
Wat zijn externe toezichthouders?  Hebben metalen een lage specifieke warmte?
Hebben metalen een lage specifieke warmte?
 Wat gebeurt er met de dieren in het regenwoud wanneer het wordt gekapt?
Wat gebeurt er met de dieren in het regenwoud wanneer het wordt gekapt?  Wat is het verschil tussen een regenwoud en jungle?
Wat is het verschil tussen een regenwoud en jungle?  Hoe strike-slip fouten ontstaan, de oorsprong van aardbevingen
Hoe strike-slip fouten ontstaan, de oorsprong van aardbevingen Schimmels kunnen worden gebruikt als biomonitors voor het beoordelen van radioactiviteit in onze omgeving
Schimmels kunnen worden gebruikt als biomonitors voor het beoordelen van radioactiviteit in onze omgeving Wat is het verschil tussen een sporen- en een stuifmeelkorrel?
Wat is het verschil tussen een sporen- en een stuifmeelkorrel?
Hoofdlijnen
- Welk product maakt voedselproductie efficiënter?
- Bacterieel model helpt onthullen hoe ons lichaam bevolkingsexplosies – en kanker – voorkomt
- Wie gebruikt de wetenschappelijke methode?
- Komt natuurlijke selectie op in genen of allelen?
- Wat zijn de vier soorten bewijsmateriaal dat de evolutie van de theorie ondersteunt?
- Waarom zijn meiose en mitose verward?
- Wat is een molecuul dat wordt geproduceerd door DNA uit twee verschillende bronnen te combineren?
- Wat is de rol van mRNA bij de eiwitsynthese?
- Een benadering van het hele lichaam om chemosensorische cellen te begrijpen
- Onderzoekers gebruiken kunstmatige neurale netwerken om het testen van materialen te stroomlijnen

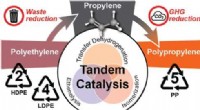
- Wetenschappers ontdekken het upcyclen van plastic om de uitstoot van broeikasgassen te verminderen
- Onderzoek levert potentiële bioblendstock op voor dieselbrandstof

- Kunstmatige antimicrobiële peptiden kunnen helpen om resistente bacteriën te overwinnen
- Biologisch proces nabootsen, hydrogel signaleert en geeft eiwitten af

 Wat is de vloeibare rots in een vulkaan die wordt genoemd?
Wat is de vloeibare rots in een vulkaan die wordt genoemd?  Kan de wetenschap, nu de bekende Cavendish-banaan in gevaar is, hem helpen overleven?
Kan de wetenschap, nu de bekende Cavendish-banaan in gevaar is, hem helpen overleven?  Waar slaan lipiden energie op?
Waar slaan lipiden energie op?  Hoe geef je een lading in een elektrisch veld potentiële energieverleners van personeel en afstand?
Hoe geef je een lading in een elektrisch veld potentiële energieverleners van personeel en afstand?  Wat is een kracht die een object in beweging zet?
Wat is een kracht die een object in beweging zet?  Wat zijn de belangrijkste bronnen van chloorradicalen?
Wat zijn de belangrijkste bronnen van chloorradicalen?  De moleculen die extracellulaire signalen omzetten in intracellulaire signalen zijn?
De moleculen die extracellulaire signalen omzetten in intracellulaire signalen zijn?  Een gebruiksvriendelijke, stapsgewijze handleiding voor het uitvoeren van vergelijkende productevaluaties
Een gebruiksvriendelijke, stapsgewijze handleiding voor het uitvoeren van vergelijkende productevaluaties
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

