
Wetenschap
Hoeveel atomen in 1,84 g BI?
1. Vind de molaire massa van Bismuth:
* De molaire massa van bismut is ongeveer 208,98 g/mol.
2. Bereken het aantal mol:
* Verdeel de massa van bismut door zijn molaire massa:
* mol Bi =1,84 g / 208,98 g / mol ≈ 0,0088 mol
3. Gebruik het nummer van Avogadro:
* Het nummer van Avogadro stelt dat er 6.022 x 10^23 atomen zijn in één mol van elke stof.
* Vermenigvuldig het aantal mol met het nummer van Avogadro:
* Atomen van Bi =0,0088 mol * 6.022 x 10^23 Atomen/mol ≈ 5,3 x 10^21 atomen
Daarom zijn er ongeveer 5,3 x 10^21 atomen in 1,84 g Bismuth.
 Waarom is het cooler op de berg?
Waarom is het cooler op de berg?  Hoe beïnvloedt luchtmassa het klimaat?
Hoe beïnvloedt luchtmassa het klimaat?
Een luchtmassa is een grote eenheid van de lagere atmosfeer die wordt gedefinieerd door gemeenschappelijke fysieke kenmerken, zoals temperatuur en vochtigheid, op elke gegeven hoogte en een die onopvallend en
 Zoete grondwaterstroming belangrijk voor kustecosystemen
Zoete grondwaterstroming belangrijk voor kustecosystemen Klimaatgasbudgetten overschatten de methaanuitstoot uit de Noordelijke IJszee sterk
Klimaatgasbudgetten overschatten de methaanuitstoot uit de Noordelijke IJszee sterk Het ijsverlies op Groenland is mogelijk al in het midden van de jaren 80 begonnen
Het ijsverlies op Groenland is mogelijk al in het midden van de jaren 80 begonnen
Hoofdlijnen
- De COVID-wiebel opvangen:Onderzoekers ontwikkelen een nieuwe manier om te visualiseren hoe spike-eiwit zijn bewegingen laat zien
- Hoe de darm een gezellig thuis creëert voor nuttige microbioomsoorten
- Team levert nieuwe basisgegevens over zeeluipaarden, mysterieuze toproofdieren van Antarctica
- Wat is de menselijke functie?
- Ziekte in het vuil:hoe schurftveroorzakende mijten een Tasmaanse wombatpopulatie hebben gedecimeerd
- Een beter begrip van gewasopbrengsten onder klimaatverandering
- Onderzoekers:Desinformatiecampagnes ondermijnen de democratie – zo kunnen we terugvechten
- Zijn mannen of vrouwen betere navigators?
- Hoe zijn selectief permeabele membranen essentieel voor het leven?
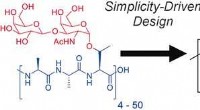
- Polyproline beschermt celmonolagen tegen vorstschade
- Materiaalwetenschappers vinden nieuwe invalshoek voor betere warmteoverdracht

- Groen materiaal voor koeling geïdentificeerd

- Nieuwe gel beschermt eieren - en misschien ooit koppen - tegen schade

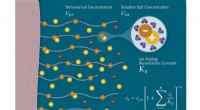
- Onderzoek beschrijft hoe ionen een sleutelrol spelen bij het beheersen van slijmvliesoppervlakken
 Nobelprijswinnende techniek zoals Google Earth voor moleculen
Nobelprijswinnende techniek zoals Google Earth voor moleculen Standpunt:Waarom ik de fouten van mijn vroege onderzoek rechtzet en wetenschappelijke gegevens deel met lokale gemeenschappen
Standpunt:Waarom ik de fouten van mijn vroege onderzoek rechtzet en wetenschappelijke gegevens deel met lokale gemeenschappen  Hoe dik is de ionosfeer?
Hoe dik is de ionosfeer?  Wat voor soort steen is Mountaine?
Wat voor soort steen is Mountaine?  Wat zijn delen van de eenvoudige circuits?
Wat zijn delen van de eenvoudige circuits?  Wat is de snelheid van een elektromagnetische golf met een frequentie 5.21 1016 Hz en golflengte 5,76 nm?
Wat is de snelheid van een elektromagnetische golf met een frequentie 5.21 1016 Hz en golflengte 5,76 nm?  Hoe verhoudt de chemische formule van een verbinding zich op relatieve nummeratomen in verbinding?
Hoe verhoudt de chemische formule van een verbinding zich op relatieve nummeratomen in verbinding?  Hoe vierkantjes in kubieke voeten te converteren
Hoe vierkantjes in kubieke voeten te converteren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

