
Wetenschap
Oriëntatie natriumionen en chloride -ionen?
Hier is hoe ze georiënteerd zijn:
* kubieke structuur: De natrium- en chloride-ionen rangschikken zichzelf in een gezichtsgerichte kubieke (FCC) rooster. Dit betekent dat elk ion is omgeven door zes ionen van de tegenovergestelde lading.
* Afwisselende kosten: Natriumionen en chloride -ionen afwisselen in het rooster. Dit creëert een evenwichtige, neutrale lading door het kristal.
* ionische bindingen: De aantrekkelijke krachten tussen de positief geladen natriumionen en de negatief geladen chloride -ionen worden ionische bindingen genoemd . Deze bindingen houden de kristalstructuur bij elkaar.
Visualisatie van de structuur:
Stel je een kubus voor. In het midden van elk gezicht van de kubus is er een natriumion. In het midden van de kubus zelf is er een chloride -ion. Dit patroon herhaalt zich in de kristalstructuur.
Sleutelpunten:
* De oriëntatie van natrium- en chloride -ionen in het kristalrooster is essentieel voor de stabiliteit van het zoutkristal.
* De sterke ionische bindingen tussen de ionen geven tafelzout zijn hoge smeltpunt en hardheid.
Opmerking: Hoewel we het hebben over de oriëntatie van ionen in een kristal, is het belangrijk om te onthouden dat ionen constant trillen in het rooster. Ze zijn niet statisch, maar hun beweging is beperkt tot een specifieke, georganiseerde opstelling.
 Eindpunten berekenen
Eindpunten berekenen  Wat gebeurt er wanneer de temperatuur van een stof aanzienlijk daalt. De meeste stoffen zullen uitzetten. B. Krijg atomen. C. Contract. D. D?
Wat gebeurt er wanneer de temperatuur van een stof aanzienlijk daalt. De meeste stoffen zullen uitzetten. B. Krijg atomen. C. Contract. D. D?  Ontdekking van een eenvoudig proces voor H2-productie met ammoniak als drager
Ontdekking van een eenvoudig proces voor H2-productie met ammoniak als drager Draagbaar apparaat verlicht de weg naar betere detectie van door voedsel overgedragen ziekten
Draagbaar apparaat verlicht de weg naar betere detectie van door voedsel overgedragen ziekten Is kopernitraat een metaal of een niet-metaal?
Is kopernitraat een metaal of een niet-metaal?
 Extreme weersomstandigheden in 2016 en banden met klimaatverandering
Extreme weersomstandigheden in 2016 en banden met klimaatverandering Mammoetjagers - weg met een gejammer of een knal?
Mammoetjagers - weg met een gejammer of een knal?  Geef alstublieft de shiraz door:hoe de Australische wijnindustrie zich kan aanpassen aan de klimaatverandering
Geef alstublieft de shiraz door:hoe de Australische wijnindustrie zich kan aanpassen aan de klimaatverandering  Hoe de popcultuur de juridische opvattingen over vloeken kan (en moet) veranderen
Hoe de popcultuur de juridische opvattingen over vloeken kan (en moet) veranderen  Wat zorgt ervoor dat de aarde seizoenen experimenteert?
Wat zorgt ervoor dat de aarde seizoenen experimenteert?
Hoofdlijnen
- Wat is het totale aantal gepaarde chromosomen in de bodycel die wordt genoemd?
- Chemische vingerafdrukken gebruiken om fraude met zeevruchten en illegale visserij te bestrijden
- Zijn baterium en bacteriën hetzelfde?
- Hyfen die horizontaal groeien langs het oppervlak van een voedselbron worden genoemd?
- Vier grote groepen organische verbindingen die levende organismen samenstellen
- Wat is het nut van chloroform in DNA -extractie uit organismen?
- Hoe vermijdt planten-DNA de verwoestingen van UV-straling?
- Onder geraniums zwaaien petunias of fuchsias die de moeilijkste bloem is?
- Wat is het organisme dat dood en levend is?
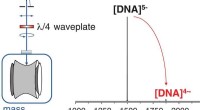
- Massaspectrometrie gebruiken om guaninerijke DNA-ionen te isoleren
- Een goedkopere manier om atomaire laagafzetting op te schalen

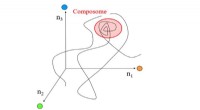
- Enzym-aangedreven protocellen stijgen naar de top
- Een eeuwenoud model voor het ontstaan van levens krijgt flinke onderbouwing
- Studie biedt nieuwe inzichten voor technologieën voor het verzamelen van de zon

 Wiskundeprojecten met behulp van cirkels
Wiskundeprojecten met behulp van cirkels  Welke uitspraken zijn juist over het effect van cultuur en biologie?
Welke uitspraken zijn juist over het effect van cultuur en biologie?  Wat is het natuurfenomeen?
Wat is het natuurfenomeen?  Wat is er in zwavel?
Wat is er in zwavel?  Welke soorten objecten worden aangetrokken door magneten?
Welke soorten objecten worden aangetrokken door magneten?  AI zet laatste aantekeningen op Beethovens Tiende symfonie
AI zet laatste aantekeningen op Beethovens Tiende symfonie Eerste catalogus van röntgenbronnen in overlappende waarnemingen gepubliceerd
Eerste catalogus van röntgenbronnen in overlappende waarnemingen gepubliceerd Dichte microgelsuspensies onthullen in-silico wat er gebeurt onder compressie
Dichte microgelsuspensies onthullen in-silico wat er gebeurt onder compressie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

