
Wetenschap
Wat is de gebalanceerde chemische vergelijking voor het verbranden van C18H38 in lucht?
2 C18H38 + 55 O2 → 36 CO2 + 38 H2O
Hier is hoe je het afbreekt:
* C18H38: Dit is de formule voor Octadecane, een type alkane.
* o2: Dit is de formule voor zuurstof, die in de lucht aanwezig is.
* CO2: Dit is de formule voor koolstofdioxide, een product van verbranding.
* h2o: Dit is de formule voor water, een ander product van verbranding.
het balanceren van de vergelijking:
* koolstof (c): Er zijn 18 koolstofatomen aan de linkerkant en 36 aan de rechterkant. We moeten de CO2 met 2 vermenigvuldigen.
* waterstof (h): Er zijn 38 waterstofatomen aan de linkerkant en 38 aan de rechterkant. De vergelijking is al in balans voor waterstof.
* zuurstof (O): Er zijn 55 zuurstofatomen aan de rechterkant en 2 aan de linkerkant. We moeten de O2 vermenigvuldigen met 55/2, wat vereenvoudigt tot 27.5. We kunnen echter geen breuken hebben in een chemische vergelijking. Daarom vermenigvuldigen we de hele vergelijking met 2 om hele getallen te krijgen.
Dit proces leidt tot de laatste evenwichtige vergelijking:
2 C18H38 + 55 O2 → 36 CO2 + 38 H2O
 Is waterstofchloride oplosbaar of onoplosbaar in organische oplosmiddelen?
Is waterstofchloride oplosbaar of onoplosbaar in organische oplosmiddelen?  Zou de dichtheid zinken of vloeren water?
Zou de dichtheid zinken of vloeren water?  Nieuwe methode biedt stabieler, efficiënte elektrokatalytische reacties
Nieuwe methode biedt stabieler, efficiënte elektrokatalytische reacties Hoe verandert het volume van een ideaal gas bij constante temperatuur en druk naarmate het aantal moleculen toeneemt?
Hoe verandert het volume van een ideaal gas bij constante temperatuur en druk naarmate het aantal moleculen toeneemt?  Wat is de oxidatietoestand voor NACUCL2?
Wat is de oxidatietoestand voor NACUCL2?
 Wat is een voorbeeld van symbiose in gematigd bladverliezend bos?
Wat is een voorbeeld van symbiose in gematigd bladverliezend bos?  Luchtvervuilingsproject maakt gebruik van de kracht van wetenschapsenthousiastelingen in de achtertuin
Luchtvervuilingsproject maakt gebruik van de kracht van wetenschapsenthousiastelingen in de achtertuin Bedreigde planten en dieren in Costa Rica
Bedreigde planten en dieren in Costa Rica  Sterke aardbeving treft eilandketen voor Nieuw-Zeeland; geen tsunami
Sterke aardbeving treft eilandketen voor Nieuw-Zeeland; geen tsunami Enge opwarming bij palen die op rare tijden verschijnen, plaatsen
Enge opwarming bij palen die op rare tijden verschijnen, plaatsen
Hoofdlijnen
- Is een kuiken prokaryotisch of eukaryotisch?
- Klimaatverandering verlengt, intensiveert de bloei van steeneik en andere Quercus-soorten:studie
- Wat is de betekenis van Wetenschap Woordweer?
- Wat zijn de verschillen tussen een virus en een parasiet?
- Van stamcellen afgeleide levercellen geven nieuwe aanwijzingen voor ebola
- Welke cel is niet gespecialiseerd?
- Bioreactorprocessen en cryotechnologieën verbeteren het testen van actieve ingrediënten met behulp van menselijke celculturen
- Komt chromosoomreplicatie op bij mitose en meiose?
- Welk percentage van een plantencel is water?
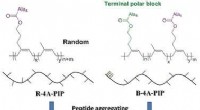
- Biomimetische strategie leidt tot sterke, recyclebaar rubber
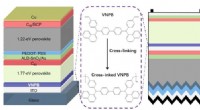
- Verknoopte gatentransportlagen voor hoogrenderende perovskiet-tandemzonnecellen
- Nieuwe moleculen voor OLED's en geneesmiddelen

- Kevers zorgen voor ontwikkeling van kleurveranderende nanodeeltjes voor commercieel gebruik

- Nieuwe methodologie helpt bij het bestuderen van veelbelovende gerichte steigers voor medicijnafgifte

 Hoe lang bestaat het noorderlicht al?
Hoe lang bestaat het noorderlicht al?  Waarom heeft magnesium een lager smelt- en kookpunt dan calciumstrontium andere leden die onder magnesium aanwezig zijn?
Waarom heeft magnesium een lager smelt- en kookpunt dan calciumstrontium andere leden die onder magnesium aanwezig zijn?  Waar is 40 graden zuid en 120 West gelegen?
Waar is 40 graden zuid en 120 West gelegen?  Waarom heeft rubidium een kleinere ionisatie -energie dan jodium?
Waarom heeft rubidium een kleinere ionisatie -energie dan jodium?  De studie van hoe omgevingsfactoren de expressiegenen beïnvloeden zonder DNA te veranderen, staat bekend als?
De studie van hoe omgevingsfactoren de expressiegenen beïnvloeden zonder DNA te veranderen, staat bekend als?  Wat is de samenvatting van een wetenschapsproject van Crystal Egg Geodes?
Wat is de samenvatting van een wetenschapsproject van Crystal Egg Geodes?  Een nieuw kader voor het koolstofbudget geeft een duidelijker beeld van onze klimaatdeadlines
Een nieuw kader voor het koolstofbudget geeft een duidelijker beeld van onze klimaatdeadlines Hoe zou een zonne -energiehuis energie krijgen op bewolkte of regenachtige dag?
Hoe zou een zonne -energiehuis energie krijgen op bewolkte of regenachtige dag?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

