
Wetenschap
Wanneer een bariumatoom het meest voorkomende ion vormt?
Dit is waarom:
* Elektronenconfiguratie: Barium (BA) heeft een elektronenconfiguratie van [XE] 6S². Dit betekent dat het twee elektronen in zijn buitenste schaal heeft.
* octetregel: Atomen hebben de neiging om elektronen te winnen, verliezen of delen om een stabiele elektronenconfiguratie te bereiken, meestal met acht elektronen in hun buitenste schaal (de octetregel).
* ionische binding: Barium is een metaal en metalen verliezen de neiging elektronen te verliezen om positieve ionen (kationen) te vormen. Om een stabiel octet te bereiken, verliest Barium gemakkelijk zijn twee buitenste shell -elektronen.
Daarom is de meest voorkomende ion van barium ba²⁺ .
 Hoe zuurstof en voedingsstoffen worden getransporteerd door oceaanstromingen?
Hoe zuurstof en voedingsstoffen worden getransporteerd door oceaanstromingen?  Wat gebeurt er als magnesium reageert met verdund zwavelzuur?
Wat gebeurt er als magnesium reageert met verdund zwavelzuur?  De meest voorkomende chemische stof in het menselijk lichaam?
De meest voorkomende chemische stof in het menselijk lichaam?  Hoe wordt CO2 gevormd in een kolencentrale en benzinestation?
Hoe wordt CO2 gevormd in een kolencentrale en benzinestation?  Wat is de totale lading van elektronen in een natriumion?
Wat is de totale lading van elektronen in een natriumion?
 Natuurlijke bronnen van extractie van gibberellinezuur
Natuurlijke bronnen van extractie van gibberellinezuur  NASA ziet Atlantische subtropische storm Melissa vormen voor de kust van New England
NASA ziet Atlantische subtropische storm Melissa vormen voor de kust van New England Onderzoek toont aan dat klimaatkoeling invloed heeft op de manier waarop menselijke samenlevingen gedijen of achteruitgaan
Onderzoek toont aan dat klimaatkoeling invloed heeft op de manier waarop menselijke samenlevingen gedijen of achteruitgaan  Wat is de verstoring van de beweging het ene hemelse lichaam door een ander geroepen?
Wat is de verstoring van de beweging het ene hemelse lichaam door een ander geroepen?  Meststoffen passen de stikstofcyclus van prairieplanten aan, volgens nieuwe studie
Meststoffen passen de stikstofcyclus van prairieplanten aan, volgens nieuwe studie
Hoofdlijnen
- Wat zal hoogstwaarschijnlijk voorkomen wanneer een cel in zoutoplossing wordt geplaatst met een hogere zoutconcentratie dan de cel?
- Is de fysieke verschijning van een organisme het?
- Wat is acetylcholinesteresce?
- Wat zijn de wortelstructuren?
- Van gist naar hypha:hoe Candida albicans de overstap maakt
- Wat is de grootte van het menselijk genoom?
- Voedsel voor onze darmen:menselijke microben voeden zich met plantensuikers
- Wat zijn enkele niet -voorbeelden van wetenschap?
- Hoe ondersteunt genetica de evolutie?
- Onderzoek naar parasieten warmt op
- Vloeibaar platina bij kamertemperatuur:de koele katalysator voor een duurzame revolutie in de industriële chemie

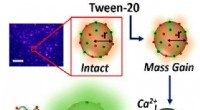
- Wetenschappers onthullen hoe wasmiddelen eigenlijk werken
- Van lint tot scroll:vormcontrole verkrijgen door elektrostatica

- De warmtestroom in een vaste stof beheersen door de dimensionaliteit van de kristalstructuur te veranderen

 Anorganische dubbele helix:een flexibele halfgeleider voor elektronica, zonnetechnologie en fotokatalyse
Anorganische dubbele helix:een flexibele halfgeleider voor elektronica, zonnetechnologie en fotokatalyse Waarom wordt steenkool de belangrijkste energiebron genoemd?
Waarom wordt steenkool de belangrijkste energiebron genoemd?  Zijn er nog andere dwergplaneten naast Pluto?
Zijn er nog andere dwergplaneten naast Pluto?  Hoe telescopen werken
Hoe telescopen werken  Onderzoekers tonen diepteafhankelijke reacties van organische koolstof in de bodem onder stikstofafzetting
Onderzoekers tonen diepteafhankelijke reacties van organische koolstof in de bodem onder stikstofafzetting  Wat is de massa zon in kilo's?
Wat is de massa zon in kilo's?  Tactisch responsieve Launch-2-lading gelanceerd in een baan om de aarde na in recordtijd te zijn gebouwd
Tactisch responsieve Launch-2-lading gelanceerd in een baan om de aarde na in recordtijd te zijn gebouwd UFO-gelovigen hebben één ding goed - dit is wat ze fout hebben
UFO-gelovigen hebben één ding goed - dit is wat ze fout hebben
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

