
Wetenschap
Wat is een voorbeeld van anorganische vorm koolstof?
* anorganische verbindingen Over het algemeen missen koolstof-hydrogen bindingen (C-H).
* diamant is een kristallijne vorm van zuivere koolstof waarbij elk koolstofatoom wordt gebonden aan vier andere koolstofatomen in een tetraëdrische opstelling. Deze structuur mist C-H-bindingen, waardoor het anorganisch is.
Andere voorbeelden van anorganische vormen van koolstof zijn onder meer:
* grafiet: Een andere kristallijne vorm van koolstof met een gelaagde structuur.
* fullereen: Een molecuul bestaande uit koolstofatomen die een holle bol, ellipsoïde of buis vormen.
* koolstofnanobuisjes: Eendimensionale cilindrische structuren van koolstofatomen.
* koolstof nanofoam: Een ultralichte, poreuze vorm van koolstof met een sponsachtige structuur.
Hoewel deze allemaal uit koolstof zijn samengesteld, classificeren hun structuren en gebrek aan C-H-bindingen ze als anorganische verbindingen.
 Wat bepaalt een benthische zone in LIKE zal fotosynthese ondersteunen?
Wat bepaalt een benthische zone in LIKE zal fotosynthese ondersteunen?  De opwarming van de aarde kan worden beperkt tot 1,5 C door de manier waarop we reizen te veranderen, warmte huizen, apparaten gebruiken
De opwarming van de aarde kan worden beperkt tot 1,5 C door de manier waarop we reizen te veranderen, warmte huizen, apparaten gebruiken Wat zijn enkele wetenschapskwaliteiten?
Wat zijn enkele wetenschapskwaliteiten?  Hoe schaadt het gebruik van natuurlijke hulpbronnen het milieu?
Hoe schaadt het gebruik van natuurlijke hulpbronnen het milieu?  Wetenschappers presenteren nieuwe methode voor teledetectie van atmosferische dynamiek
Wetenschappers presenteren nieuwe methode voor teledetectie van atmosferische dynamiek
Hoofdlijnen
- Bacteriën zijn de eenvoudigste enkele cellen die?
- Wat is higogeen?
- Waar komt in het menselijk lichaam osmose op?
- Ontwikkelen planten- en diercellen een celplaat?
- Wat is de term steriel?
- Welk deel van de uienplant dient als opslagorgel?
- Onderzoekers laten zien dat mobiele elementen rond het genoom apen
- Wat is de formule voor productwetgeving in de biologie?
- Waarom komen sekschromosoomafwijkingen vaker voor?
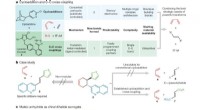
- Het beste van twee werelden:twee skeletvormende chemische reacties combineren
- Onderzoekers produceren filamenten en vezels die drie keer fijner zijn dan een mensenhaar
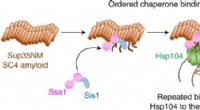
- Drie begeleiders coördineren het uiteenvallen van amyloïde fibrillen in gist
- Draagbare elektronica voor continue cardiale, ademhalingsbewaking

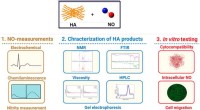
- Onderzoekers gebruiken stikstofmonoxidevangers om triple-negatieve borstkanker aan te pakken
 India laat Huawei deelnemen aan 5G-proeven
India laat Huawei deelnemen aan 5G-proeven Wat bevat een waterstofatoom dat een elektron heeft verloren?
Wat bevat een waterstofatoom dat een elektron heeft verloren?  Eerste muziekfestival verandert in blockchain
Eerste muziekfestival verandert in blockchain Waarom het bezoeken van door de overheid gefinancierde scholen studenten kan helpen cultureel gevoeliger te worden
Waarom het bezoeken van door de overheid gefinancierde scholen studenten kan helpen cultureel gevoeliger te worden  ALICE registreert ongeveer 12 miljard botsingen met zware ionen
ALICE registreert ongeveer 12 miljard botsingen met zware ionen  'S Werelds langste spoorbaan van sauropod-dinosaurussen aan het licht gebracht
'S Werelds langste spoorbaan van sauropod-dinosaurussen aan het licht gebracht Zelfsorterend door moleculaire geometrieën
Zelfsorterend door moleculaire geometrieën Eerste EPA-goedgekeurde buitenveldproef voor genetisch gemanipuleerde algen
Eerste EPA-goedgekeurde buitenveldproef voor genetisch gemanipuleerde algen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

