
Wetenschap
Water wordt beschouwd als een zuur omdat het waterstofionen vrijgeeft?
Die verklaring is niet helemaal nauwkeurig . Hoewel water waterstofionen (H+) kan vrijgeven, geeft het ook hydroxide-ionen vrij (OH-), waardoor het amfiprotisch is .
Dit is waarom:
* Autoionisatie van water: Watermoleculen kunnen met elkaar reageren in een proces dat autoionisatie wordt genoemd:
2h₂o ⇌ H₃o⁺ + oh⁻
* Gelijke concentraties: In zuiver water zijn de concentraties van H₃o⁺ en OH⁻ gelijk, wat resulteert in een neutrale pH van 7.
* amfiprotische aard: Water kan zowel een zuur als een basis werken. Het kan een proton (H+) doneren aan een sterkere basis, die als zuur werkt. Het kan ook een proton accepteren van een sterker zuur, dat als basis werkt.
Daarom wordt het water, hoewel water kan afgeven, niet als een zuur beschouwd omdat het ook hydroxide -ionen in gelijke concentraties vrijgeeft.
 Welk metaal verliest het gemakkelijkst elektronen natrium of kalium?
Welk metaal verliest het gemakkelijkst elektronen natrium of kalium?  Wat voor soort chemische binding wordt gevonden in een legering?
Wat voor soort chemische binding wordt gevonden in een legering?  Is de vertering van voedsel fysieke verandering of chemische verandering?
Is de vertering van voedsel fysieke verandering of chemische verandering?  Wat zijn de twee moleculen geproduceerd in lichte reactie?
Wat zijn de twee moleculen geproduceerd in lichte reactie?  Hoe te berekenen Percentage Abundances
Hoe te berekenen Percentage Abundances
 Zwitserse autoriteiten waarschuwen voor instorting gletsjer gebied evacueren
Zwitserse autoriteiten waarschuwen voor instorting gletsjer gebied evacueren NASA lanceert diepgaand sneeuwonderzoek - voor het eerst in 30 jaar
NASA lanceert diepgaand sneeuwonderzoek - voor het eerst in 30 jaar Hoe kakkerlakken eruit zien?
Hoe kakkerlakken eruit zien?  Mensen recyclen meer als ze weten wat recyclebaar afval wordt
Mensen recyclen meer als ze weten wat recyclebaar afval wordt Nieuw onderzoek laat zien hoe de opwarming van de aarde onze regenval in de war brengt
Nieuw onderzoek laat zien hoe de opwarming van de aarde onze regenval in de war brengt
Hoofdlijnen
- Hoe pest werkt
- Wat is wetenschappelijke evolutie?
- Wat kan worden toegevoegd om de bacteriegroei op schimmelgebaseerde media te onderdrukken?
- Jesse keek naar een cel via microscoop en zag mitochondria membranen wat zou kunnen zeggen over de cel?
- Waarom is de mitochondriënplaats van aerobe cellulaire ademhaling?
- Kan meiose nieuwe haarcellen creëren?
- Hoe ontwikkelen en veranderen wetenschappelijke theorieën?
- Een studie schakelt over van genetische naar metabole analyse om het evolutionaire proces te reconstrueren
- Is het evolutieproces waarmee de persoon die het beste zijn aangepast, overleven en zich voortplanten?
- Onderzoekers ontdekken een manier om de kleur van OLED's te controleren
- Prestatievezel met van kleur veranderende coating maakt mechanische belasting zichtbaar

- Onderzoekers lossen controverse op over energiekloof van Van der Waals-materiaal

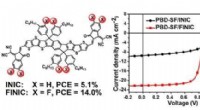
- Onderzoekers ontwikkelen elektronenacceptor met gefuseerde ring met 3D-exciton en ladingstransport
- Hulpmiddelen voor machine learning bij het ontwerpen van materialen

 Bewijs dat energiemetabolisme en regulatie van biofilmvorming in bacteriën met elkaar verweven zijn
Bewijs dat energiemetabolisme en regulatie van biofilmvorming in bacteriën met elkaar verweven zijn Zeldzame metalen op Mars en aarde impliceren kolossale effecten
Zeldzame metalen op Mars en aarde impliceren kolossale effecten Hubble en Spitzer werken samen om een vergroot en uitgestrekt beeld van een verre melkweg te vinden
Hubble en Spitzer werken samen om een vergroot en uitgestrekt beeld van een verre melkweg te vinden Kunstmatige controle van exciplexen opent mogelijkheden voor nieuwe elektronica
Kunstmatige controle van exciplexen opent mogelijkheden voor nieuwe elektronica Welke gebeurtenissen vormen de nebulaire hypothese?
Welke gebeurtenissen vormen de nebulaire hypothese?  Is het stroomverbruik van airconditioner anders bij temperaturen?
Is het stroomverbruik van airconditioner anders bij temperaturen?  Afrika heeft betere wetenschappelijke capaciteit nodig om milieu-uitdagingen aan te gaan
Afrika heeft betere wetenschappelijke capaciteit nodig om milieu-uitdagingen aan te gaan Hoe DNA -pakket zelf?
Hoe DNA -pakket zelf?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

