
Wetenschap
Waarom is de reactie SO2 plus H2O H2SO2 niet in balans?
reactanten:
* s: 1 atoom
* o: 3 atomen (2 van SO2 en 1 van H2O)
* h: 2 atomen
producten:
* s: 1 atoom
* o: 2 atomen
* h: 2 atomen
Het probleem: Er zijn 3 zuurstofatomen aan de kant van de reactanten en slechts 2 aan de productzijde.
Om de vergelijking in evenwicht te brengen, moet u de coëfficiënten voor de chemische formules aanpassen:
SO2 + H2O -> H2SO3
Verklaring van de evenwichtige vergelijking:
* SO2: 1 molecuul (1 zwavelatoom en 2 zuurstofatomen)
* h2o: 1 molecuul (2 waterstofatomen en 1 zuurstofatoom)
* H2SO3: 1 molecuul (2 waterstofatomen, 1 zwavelatoom en 3 zuurstofatomen)
Nu is de vergelijking in evenwicht:
* s: 1 atoom aan elke kant
* o: 3 atomen aan elke kant
* h: 2 atomen aan elke kant
Belangrijke opmerking: Het product van de reactie is eigenlijk zwavelzuur (H2SO3) , niet H2SO2 .
 Het driekoolstofmolecuul waaraan functionele lipiden zijn gekoppeld, wordt genoemd?
Het driekoolstofmolecuul waaraan functionele lipiden zijn gekoppeld, wordt genoemd?  Hoe leg je de uitdrukking als oplost in termen van polaire en niet -polaire stoffen?
Hoe leg je de uitdrukking als oplost in termen van polaire en niet -polaire stoffen?  Het mechanisme van foto-geëxciteerde nucleobasen blootleggen:is verval snel of onderdrukt?
Het mechanisme van foto-geëxciteerde nucleobasen blootleggen:is verval snel of onderdrukt?  Wat is het verschil tussen diffusie en osmose?
Wat is het verschil tussen diffusie en osmose?  Wat is G2P1001?
Wat is G2P1001?
 Deken van rotspuin biedt gletsjers meer bescherming tegen klimaatverandering dan eerder bekend
Deken van rotspuin biedt gletsjers meer bescherming tegen klimaatverandering dan eerder bekend Overstromingen in Delhi terwijl de moessontol in Zuid-Azië oploopt tot bijna 1. 300
Overstromingen in Delhi terwijl de moessontol in Zuid-Azië oploopt tot bijna 1. 300 Dacht je dat de olieramp erg was? in LA, giftig afval is overal
Dacht je dat de olieramp erg was? in LA, giftig afval is overal Minister belooft schone lucht in Delhi in drie jaar
Minister belooft schone lucht in Delhi in drie jaar Nieuw briefingdocument over Arctische verandering
Nieuw briefingdocument over Arctische verandering
Hoofdlijnen
- Wat is de wetenschappelijke gemeenschappelijke naam voor gastro -intestinale ziekte?
- Vis uit het water:hoe killifish-embryo's hun ontwikkeling aanpassen
- Wat voor soort dinoflagellaat heeft rode fotosynthetische pigmenten?
- Haaienvinnenverboden helpen haaien misschien niet, wetenschappers zeggen:
- Onderzoek onderzoekt hoe druivenplagen bessen opsnuiven
- Wat kunnen fruitvliegjes ons leren over hoe wezens voedsel vinden?
- Wat is een biomembraan?
- De vetten die in je lichaam zijn opgeslagen, bestaan meestal uit?
- Wat is het totale aantal gepaarde chromosomen in de bodycel die wordt genoemd?
- hoe vitamines, steroïden en mogelijke antivirale middelen kunnen SARS-CoV-2 beïnvloeden

- Zelfherstellend materiaal een doorbraak voor bio-geïnspireerde robotica

- De vorm van water ontsluiten in mechanismen van antibioticaresistentie

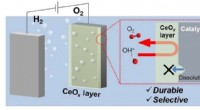
- Zuurstofproductie afschermen om waterstof aan te houden
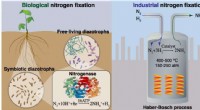
- Groenere benaderingen van stikstofbinding verkennen
 Waar komen ondiepe aardbevingen voor?
Waar komen ondiepe aardbevingen voor?  Erven alle planten één dominant allel?
Erven alle planten één dominant allel?  Conserveringsbioloog zegt dat het nu tijd is om op te treden voor de Amazone
Conserveringsbioloog zegt dat het nu tijd is om op te treden voor de Amazone Bosnische stad Mostar overspoeld met afval tijdens protest tegen stortplaatsen
Bosnische stad Mostar overspoeld met afval tijdens protest tegen stortplaatsen Welke worstvormige cellen regelen de grootte van openingen waarmee koolstofdioxide en zuurstof in een blad kunnen gaan?
Welke worstvormige cellen regelen de grootte van openingen waarmee koolstofdioxide en zuurstof in een blad kunnen gaan?  Wat is een helder gebied op het oppervlak van de zon die wordt genoemd?
Wat is een helder gebied op het oppervlak van de zon die wordt genoemd?  Op de hightech Tokyo Game Show, old skool zijn de beste
Op de hightech Tokyo Game Show, old skool zijn de beste Naaldboom die geurig is, vaak rood gekleurd hout?
Naaldboom die geurig is, vaak rood gekleurd hout?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

