
Wetenschap
Ethanol CH3CHO - Hoe een vergelijking te schrijven vertegenwoordigt de enthalpie van de vorming?
Inzicht in de enthalpie van formatie
De enthalpie van de vorming (ΔHF °) is de verandering in enthalpie die optreedt wanneer een mol van een verbinding wordt gevormd uit zijn elementen in hun standaardstaten onder standaardomstandigheden (meestal 25 ° C en 1 atm).
het schrijven van de vergelijking
1. Identificeer de elementen: Ethanol wordt gevormd uit koolstof (C), waterstof (H₂) en zuurstof (O₂).
2. Standaard staat:
* Koolstof bestaat als vast grafiet (C (s)).
* Waterstof bestaat als diatomisch gas (H₂ (G)).
* Zuurstof bestaat als diatomisch gas (o₂ (g)).
3. Breng de vergelijking in evenwicht:
`` `
2 c (s) + 3 H₂ (g) + 1/2 o₂ (g) → c₂h₅oh (l)
`` `
Enthalpy Change (ΔHF °)
De enthalpie van de vorming van ethanol is de enthalpieverandering (ΔH) geassocieerd met deze reactie. Het wordt meestal uitgedrukt in eenheden van kj/mol. U kunt de standaard enthalpie opzoeken van de vorming van ethanol in een tabel met thermodynamische gegevens.
belangrijke opmerkingen:
* Standaard stelt: Zorg er altijd voor dat u de standaardstaten van de elementen gebruikt.
* staten van materie: Neem de staten van materie (s, l, g, aq) op voor elke stof.
* Coëfficiënt: De ethanolcoëfficiënt moet 1 mol zijn volgens de definitie van enthalpie van vorming.
* Enthalpy of Formation is een specifieke waarde: De enthalpie van formatie is een specifieke waarde voor een verbinding en wordt meestal gegeven in thermodynamische gegevenstabellen.
Laat het me weten als je nog andere vragen hebt!
 Slechts 1 op de 10 van 's werelds grootste energiebedrijven heeft plannen gemaakt om tot nul uitstoot te komen
Slechts 1 op de 10 van 's werelds grootste energiebedrijven heeft plannen gemaakt om tot nul uitstoot te komen Wetenschappers verbeteren hoe wereldwijde klimaatvooruitgang kan worden berekend
Wetenschappers verbeteren hoe wereldwijde klimaatvooruitgang kan worden berekend Hoe je de Bijbel leest, hangt samen met de opleiding van medeaanbidders, ontdekt de onderzoeker
Hoe je de Bijbel leest, hangt samen met de opleiding van medeaanbidders, ontdekt de onderzoeker  Oceanografen lossen mysterie van overleving van fytoplankton op in voedselarme Stille Oceaan
Oceanografen lossen mysterie van overleving van fytoplankton op in voedselarme Stille Oceaan Soorten Arizona wilde katten
Soorten Arizona wilde katten
Hoofdlijnen
- Hoe erven iemand eigenschap zoals haartextuur?
- Lijst van aseksueel reproducerende organismen
- Pesticiden en slechte voeding schaden de diergezondheid
- Wat zijn de belangrijkste pars van je lichaam?
- Hoe kun je zien of wasmiddel biologisch is of niet?
- Wat is de functie van microbiologie?
- Welke celstructuur wordt gemaakt in G1?
- Wat is microbiële transformatie van steroïden en de betekenis ervan?
- Een extracellulaire matrix wordt geproduceerd door glycoproteïne -secretie Wat?
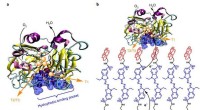
- Verbetering van de elektronenoverdracht in enzymatische biobrandstofcellen
- Licht als hulpmiddel voor de synthese van complexe moleculen

- Atomaire structuur van aluminiumlegeringen bestuderen voor de fabricage van moderne vliegtuigen

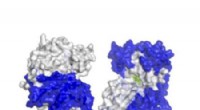
- Ontwikkeling van een enzym tegen antibioticaresistente miltvuur
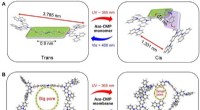
- Microporeuze polymeermembranen voor licht-gated ionentransport
 Hoeveel neutronen heeft Strontium 90?
Hoeveel neutronen heeft Strontium 90?  Welke rol speelt cytokinese tijdens de celcyclus?
Welke rol speelt cytokinese tijdens de celcyclus?  Wat is de wetenschappelijke naam voor eencellig?
Wat is de wetenschappelijke naam voor eencellig?  SpaceX bouwt een spionagesatellietnetwerk voor de VS, zegt persbureau
SpaceX bouwt een spionagesatellietnetwerk voor de VS, zegt persbureau  SpaceX klaar om geheime Zuma-missie te lanceren
SpaceX klaar om geheime Zuma-missie te lanceren Waar is 46 North Latitude en 115 West Loogte?
Waar is 46 North Latitude en 115 West Loogte?  Hier en weg:uitgaande kometen zijn waarschijnlijk van extra-solaire oorsprong
Hier en weg:uitgaande kometen zijn waarschijnlijk van extra-solaire oorsprong Wat maakt eiwitten driedimensionaal?
Wat maakt eiwitten driedimensionaal?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

