
Wetenschap
Waarom is de formule van kwikchloride hg2cl2 maar niet hgcl?
1. Kwik ionen bestaan als diatomaire kationen (hg₂²⁺):
* Mercurius (i) ionen, ook bekend als kwik ionen, zijn ongebruikelijk omdat ze bestaan als diatomaire kationen, wat betekent dat twee kwikatomen samen met een +2 lading worden gebonden.
* Dit komt door de sterke covalente binding tussen de twee kwikatomen.
2. Ladingneutraliteit handhaven:
* Om de +2 lading van het diatomic hg₂²⁺ ion in evenwicht te brengen, zijn twee chloride -ionen (CL⁻) vereist, wat resulteert in de formule HG₂CL₂.
3. HGCL is geen stabiele verbinding:
* De hypothetische verbinding hgcl zou een kwik (i) chloride zijn met een +1 lading op het kwikatoom.
* Mercurius (I) bestaat echter meestal als Hg₂²⁺ en HgCl is geen stabiele verbinding onder normale omstandigheden.
Samenvattend: De formule Hg₂cl₂ weerspiegelt nauwkeurig het bestaan van het diatomee kwikion (Hg₂²⁺) en de noodzaak om ladingsneutraliteit in de verbinding te behouden.
 Maak een lijst van enkele wetenschappelijke principes of dieptepunten?
Maak een lijst van enkele wetenschappelijke principes of dieptepunten?  Welk molecuul kan als basis functioneren?
Welk molecuul kan als basis functioneren?  Waarom zou alleen vers voorbereide oplossing van ijzersulfaat worden gebruikt?
Waarom zou alleen vers voorbereide oplossing van ijzersulfaat worden gebruikt?  Fasegrensregulering die de elektrochemische reactiviteit van op tin gebaseerde anodes voor magnesium-ionbatterijen stimuleert
Fasegrensregulering die de elektrochemische reactiviteit van op tin gebaseerde anodes voor magnesium-ionbatterijen stimuleert Nieuw onderzoek zou een meer – en efficiëntere – synthese van metastabiele materialen mogelijk kunnen maken
Nieuw onderzoek zou een meer – en efficiëntere – synthese van metastabiele materialen mogelijk kunnen maken
 Schotland zou 's werelds eerste rewilding-natie kunnen worden
Schotland zou 's werelds eerste rewilding-natie kunnen worden  Nieuw onderzoek onthult dat oceaangolven een grotere rol spelen bij het vasthouden van koolstofdioxide
Nieuw onderzoek onthult dat oceaangolven een grotere rol spelen bij het vasthouden van koolstofdioxide Orkaan Nicole werpt licht op hoe stormen diepe oceaan beïnvloeden
Orkaan Nicole werpt licht op hoe stormen diepe oceaan beïnvloeden Cyprus-studie toont grote daling van verontreinigende stoffen tijdens lockdown
Cyprus-studie toont grote daling van verontreinigende stoffen tijdens lockdown De milieu-impact van de wereldwijde gebouwde omgevingssector verminderen
De milieu-impact van de wereldwijde gebouwde omgevingssector verminderen
Hoofdlijnen
- Waarom sommige mensen muggenmagneten zijn
- Waar in de cel worden enzymen gevonden die reacties van glycolyse katalyseren?
- Indringende vraag:Moet de samenleving reproductieve technologieën reguleren?
- Wie heeft sportdranken uitgevonden?
- Maak kennis met de oudste dierlijke afstamming van Madagascar, een draaimolenkever met een 206 miljoen jaar oude oorsprong
- Welke macromoleculen voedt bijna alle levende cellen?
- Wat is het dikke buitenmembraan van acoliet?
- Wat doen micro -organismen die ervoor zorgen dat voedsel nodig is?
- Hoe MRNA naar TRNA te vertalen
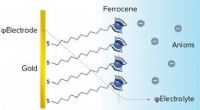
- Gecombineerde aanpak om grensvlakelektrochemie in meer detail te onderzoeken
- Enkele nanodeeltjes kunnen de weg vrijmaken voor geneesmiddelen op aanvraag

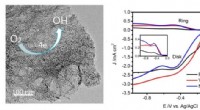
- Nieuwe elektrokatalysator ontwikkeld voor zuurstofreductiereactie
- Een nikkelkatalysator met koolwaterstoffen gebruiken om vetzuren te maken

- Implantaatinfecties kunnen worden uitgebannen dankzij doorbraak in steigers
 I-maginaire telefoon:iPhone als handtelefoon? (met video)
I-maginaire telefoon:iPhone als handtelefoon? (met video)  Backcountry skiërs opgelet:wetenschappers willen je hulp
Backcountry skiërs opgelet:wetenschappers willen je hulp Satellieten, supercomputers, en machine learning bieden realtime gegevens over het gewastype
Satellieten, supercomputers, en machine learning bieden realtime gegevens over het gewastype Verpleegster of zorg voor een wild babykonijn
Verpleegster of zorg voor een wild babykonijn  Hoe zou men de tweede wet van Newtons converteren, is gelijk aan MA van Metric?
Hoe zou men de tweede wet van Newtons converteren, is gelijk aan MA van Metric?  Een gestresste baas is een slechte baas, onderzoek concludeert
Een gestresste baas is een slechte baas, onderzoek concludeert De variaties in verhoging van een landoppervlak?
De variaties in verhoging van een landoppervlak?  Hoe vaak komt er een zonsverduistering?
Hoe vaak komt er een zonsverduistering?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

