
Wetenschap
Waarom is de vorming van chloor geclassificeerd als oxidatie?
Dit is waarom:
* oxidatie is het proces van het verliezen van elektronen.
* reductie is het proces van het verkrijgen van elektronen.
Bij de vorming van chloorgas treedt de volgende reactie op:
2 Cl⁻ → Cl₂ + 2e⁻
* chloride -ionen (Cl⁻) Elk heeft een lading van -1, wat betekent dat ze één elektron hebben gekregen.
* Bij de vorming van chloorgas (Cl₂) verliezen ze Deze elektronen worden neutrale chlooratomen.
* Deze neutrale chlooratomen binden vervolgens aan elkaar om chloorgas te vormen.
Aangezien de chloride -ionen elektronen verliezen, is dit proces geclassificeerd als oxidatie.
Het is belangrijk om te onthouden dat oxidatie en reductie altijd samen voorkomen in een proces dat redox -reactie wordt genoemd . In dit geval worden de chloorionen geoxideerd terwijl iets anders wordt verminderd. Dit kan een ander element of verbinding zijn dat de elektronen die verloren zijn gegaan door de chloride -ionen wint.
 Vaste deeltjes in de atmosfeer omvatten zout en?
Vaste deeltjes in de atmosfeer omvatten zout en?  COP24:Hoe een plasticverdrag onze oceanen zou kunnen opruimen
COP24:Hoe een plasticverdrag onze oceanen zou kunnen opruimen  Waarom doet citroenzuur penningen schoon?
Waarom doet citroenzuur penningen schoon?  Wat zijn twee belangrijke stoffen die aanwezig moeten zijn voor geleiding?
Wat zijn twee belangrijke stoffen die aanwezig moeten zijn voor geleiding?  Wat is een Coommon -oplosmiddel dat kinderen materiaal en shiff spreacteren?
Wat is een Coommon -oplosmiddel dat kinderen materiaal en shiff spreacteren?
 Dieren die afhankelijk zijn van Tides for Survival
Dieren die afhankelijk zijn van Tides for Survival  Extreme zeespiegels zullen naar verwachting langs de wereldwijde kustlijnen stijgen
Extreme zeespiegels zullen naar verwachting langs de wereldwijde kustlijnen stijgen Klimaatverandering maakt oceaangolven krachtiger, dreigt vele kustlijnen te eroderen
Klimaatverandering maakt oceaangolven krachtiger, dreigt vele kustlijnen te eroderen Wat nu voor het door cycloon getroffen Mozambique?
Wat nu voor het door cycloon getroffen Mozambique? Het Zwarte Woud en klimaatverandering
Het Zwarte Woud en klimaatverandering
Hoofdlijnen
- Van gist leren onderzoekers hoe populaties instorten
- Wat is het belang van voedselwetenschap?
- Wat zijn drie dingen die nodig zijn om fotosynthese te laten plaatsvinden?
- Wat is de relatie tussen fysiologische en genetische differentiatiebacteriën met betrekking tot taxonomische classificatie van bacteriën?
- Hoe evolueerde het hogere leven? Wetenschappers bepalen de volledige genoomsequentie van bruine alg
- Wat is de functie van een eicel?
- Wat is de studie van hoe genen worden overgedragen van ouders naar hun kinderen en rol bij gezondheidsziekten die bekend staan als?
- Hoe worden cellen gerangschikt van de kleinste naar de grootste?
- Wat is het levensmodel?
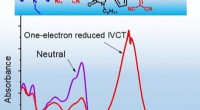
- Ingeschakelde IR-actieve organische pigmenten
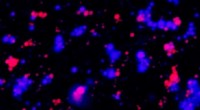
- Wetenschappers vragen:hoe kunnen vloeibare organellen in cellen naast elkaar bestaan zonder te versmelten?
- Technologie die eiwitstabiliteit voorspelt, is vrijgegeven door een spin-outbedrijf van een Britse universiteit

- Meervoudig mierachtig transport van neuronale lading door motoreiwitten

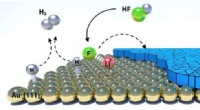
- Batterijen verborgen laag onthuld
 Hoe wordt het genoemd als de planeten om de 100 jaar aansluiten?
Hoe wordt het genoemd als de planeten om de 100 jaar aansluiten?  Wat is het percentage zwavel in chalcopyriet?
Wat is het percentage zwavel in chalcopyriet?  Opwarming van de aarde onder 1,5 graad nog steeds mogelijk, maar we moeten snel en drastisch handelen
Opwarming van de aarde onder 1,5 graad nog steeds mogelijk, maar we moeten snel en drastisch handelen Meten van verbetering in het ontwerp van pulsen voor kwantumsystemen
Meten van verbetering in het ontwerp van pulsen voor kwantumsystemen  Parijse onderzoekers beginnen Ethiopische jetrecorder te bestuderen
Parijse onderzoekers beginnen Ethiopische jetrecorder te bestuderen Leg uit waarom de celademhaling wordt gecontroleerd door enzymen?
Leg uit waarom de celademhaling wordt gecontroleerd door enzymen?  Wat is de massa van een object als Force Gravity op zijn 1033 Newtons werkt?
Wat is de massa van een object als Force Gravity op zijn 1033 Newtons werkt?  Hoe de oerknaltheorie werkt
Hoe de oerknaltheorie werkt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

