
Wetenschap
Is koolstofmetaal niet -metaal of metalloïde?
Dit is waarom:
* Gebrek aan metalen eigenschappen: Koolstof heeft niet de typische kenmerken van metalen, zoals:
* Glans (glans)
* Kneedbaarheid (vermogen om in dunne vellen te worden gehamerd)
* Ductiliteit (mogelijkheid om in draden te worden getrokken)
* Goede geleidbaarheid van warmte en elektriciteit
* vormt covalente bindingen: Koolstof vormt voornamelijk covalente bindingen met andere elementen, het delen van elektronen in plaats van te verliezen of te winnen zoals metalen doen.
* bestaat in verschillende vormen: Koolstof kan in verschillende vormen bestaan, waaronder grafiet (zacht en glad), diamant (hardste natuurlijk materiaal) en fullerenen (kooiachtige structuren). Deze diverse vormen duiden verder op zijn niet -metalen aard.
Hoewel koolstof zich soms kan gedragen op manieren die in bepaalde situaties lijken op metalen, is het fundamenteel gecategoriseerd als een niet -metaal.
Hoofdlijnen
- Het belang van diffusie in organismen
- De volgorde van de bases langs een gen bepaalt in welke?
- Wat betekent door wetenschapstechnologie en superstation te definiëren?
- Welk aminozuur is aanwezig in wateroplosbaar globulair eiwit?
- Hoe verschillen schimmelsporen van bacteriële endosporen?
- Roots rock:chimpansees drummen op hun eigen kenmerkende beats
- Hoe algenbiodiesel werkt
- Waarom zorgt normale mitose voor het leven?
- Wat zijn 2 manieren waarop wetenschappers resultaten delen?
- Natuurlijke blauwe voedselkleuring krijgt een milieuvriendelijke productieboost

- Moedermelk als hulpmiddel voor medicijnafgifte

- Surströmming:de geheimen van deze stinkende Zweedse vis

- Gluten in tarwe:wat is er veranderd in 120 jaar fokken?

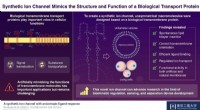
- Wetenschappers synthetiseren nieuwe kunstmatige moleculen die een celmembraaneiwit nabootsen
 Hoe ver is de volgende dichtstbijzijnde ster weg?
Hoe ver is de volgende dichtstbijzijnde ster weg?  Guardians of Apollo:de curatoren die de erfenis van de maanmissies bewaren
Guardians of Apollo:de curatoren die de erfenis van de maanmissies bewaren Hoe aardbevingen ziekenhuizen beïnvloeden:inzichten uit de aardbevingsreeksen in Turkije in 2023
Hoe aardbevingen ziekenhuizen beïnvloeden:inzichten uit de aardbevingsreeksen in Turkije in 2023  Wat gebeurt er met de snelheid van een deeltje naarmate de temperatuur afneemt?
Wat gebeurt er met de snelheid van een deeltje naarmate de temperatuur afneemt?  Waarom brengen grote stormen zoveel meer regen? Opwarming, ja, maar ook wind
Waarom brengen grote stormen zoveel meer regen? Opwarming, ja, maar ook wind  Speeding star geeft nieuwe aanwijzingen voor het uiteenvallen van multi-star systeem
Speeding star geeft nieuwe aanwijzingen voor het uiteenvallen van multi-star systeem Een cool alternatief voor airconditioning
Een cool alternatief voor airconditioning Hackers hebben toegang tot uw mobiele en laptopcamera's en kunnen u opnemen:verberg ze nu
Hackers hebben toegang tot uw mobiele en laptopcamera's en kunnen u opnemen:verberg ze nu
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


