
Wetenschap
Waarom vermindert de aanwezigheid van dubbele bindingen het smeltpunt?
Factoren die het smeltpunt beïnvloeden:
* intermoleculaire krachten: De sterkte van de aantrekkelijke krachten tussen moleculen bepaalt hoeveel energie nodig is om ze te overwinnen en over te gaan naar de vloeibare toestand. Sterkere intermoleculaire krachten leiden tot hogere smeltpunten.
* Moleculaire verpakking: Hoe goed moleculen in een vaste toestand kunnen inpakken, beïnvloedt ook het smeltpunt. Efficiënte verpakking leidt tot sterkere intermoleculaire interacties en een hoger smeltpunt.
* Symmetrie: Meer symmetrische moleculen hebben de neiging om efficiënter in te pakken, wat leidt tot hogere smeltpunten.
* kettinglengte: Langere ketens leiden in het algemeen tot hogere smeltpunten als gevolg van verhoogd oppervlak voor intermoleculaire interacties.
* Positie en geometrie van dubbele binding: De aanwezigheid van een dubbele binding kan zowel intermoleculaire krachten als moleculaire verpakking beïnvloeden.
Hoe dubbele bindingen het smeltpunt kunnen beïnvloeden:
* Verhoogde stijfheid: Dubbele bindingen zijn minder flexibel dan enkele bindingen, die de moleculaire beweging kunnen beperken en het voor moleculen moeilijker kunnen maken om strak in te pakken. Deze kan zakken het smeltpunt.
* Verhoogde polariteit: Dubbele bindingen kunnen polariteit introduceren in een molecuul, waardoor dipool-dipool interacties toenemen en mogelijk verhogen het smeltpunt.
* vervoeging: Wanneer dubbele bindingen zijn geconjugeerd (afwisselende enkele en dubbele bindingen), kunnen ze deelnemen aan gedelokaliseerde PI-elektronensystemen. Deze systemen kunnen intermoleculaire krachten verbeteren en verhogen het smeltpunt.
* sterische hindering: De aanwezigheid van een dubbele binding kan sterische hinder maken, waardoor moleculen niet efficiënt inpakken en verlagen het smeltpunt.
Voorbeelden:
* alkenes vs. alkanes: Alkenen met dubbele bindingen hebben doorgaans lager smeltpunten dan hun bijbehorende alkanen. Dit komt omdat de stijfheid van de dubbele binding de verpakkingsefficiëntie vermindert.
* cis versus trans -isomeren: Cis isomeren hebben vaak lager Smeltpunten dan trans -isomeren. Dit komt door de sterische hinder veroorzaakt door de groepen aan dezelfde zijde van de dubbele binding, waardoor efficiënte verpakking wordt voorkomen.
* geconjugeerde versus niet-geconjugeerde systemen: Geconjugeerde systemen zoals geconjugeerde Dienen hebben vaak hoger Smeltpunten dan niet-geconjugeerde systemen vanwege sterkere intermoleculaire interacties.
Conclusie:
Het effect van dubbele bindingen op het smeltpunt is complex en hangt af van het specifieke molecuul en de opstelling van de dubbele bindingen. Het is niet alleen een kwestie van dubbele bindingen die altijd het smeltpunt verlaagden. U moet rekening houden met de specifieke factoren die spelen om het smeltpunt van een molecuul dat dubbele bindingen bevat te voorspellen.
 3D-beeldvorming van oppervlaktechemie in opsluiting
3D-beeldvorming van oppervlaktechemie in opsluiting Waarom worden sommige ionen polyatomische ionen genoemd?
Waarom worden sommige ionen polyatomische ionen genoemd?  Chemische reacties kunnen zowel kwantuminformatie als zwarte gaten door elkaar gooien
Chemische reacties kunnen zowel kwantuminformatie als zwarte gaten door elkaar gooien  Welke observaties maak je bij het reageren van kaliumhydroxide met natriumcarbonaat?
Welke observaties maak je bij het reageren van kaliumhydroxide met natriumcarbonaat?  Wat wordt er gevormd als cuso4 n naoh wordt gebruikt voor een eiwittest?
Wat wordt er gevormd als cuso4 n naoh wordt gebruikt voor een eiwittest?
 Wat zijn de oorzaken van de rivierverontreiniging Pasig?
Wat zijn de oorzaken van de rivierverontreiniging Pasig?  Afbeelding:Zware regenval in Lake Success, Californië
Afbeelding:Zware regenval in Lake Success, Californië Nieuwe onderzeese kaarten leiden tot ontdekkingen van hydrothermale bronnen en soorten
Nieuwe onderzeese kaarten leiden tot ontdekkingen van hydrothermale bronnen en soorten Hoe stimuleert groene energie de bedrijfsgroei?
Hoe stimuleert groene energie de bedrijfsgroei?  Toenemende diversiteit en participatie van de gemeenschap in milieutechniek
Toenemende diversiteit en participatie van de gemeenschap in milieutechniek
Hoofdlijnen
- Schrijf naar basiseigenschappen van Nuron?
- Getoonde chimpansees die spontaan om de beurt een cijferpuzzel oplossen
- Wat COVID-19 viskwekerijen kan leren
- Wat is een functie van Cell Menbrain?
- Hoe heeft Louis Pasteur zich verhouden tot de ontwikkeling van genetische?
- Biologie 10e klas Guide of Chapter Life Processes?
- Hoe Brain Mapping werkt
- Wat is niet een manier waarop celdeling de groeiproblemen oplost?
- Waarom zou evolutie vouwen als de hele populatie dezelfde genetische make -up had?
- Nieuwe kleurstoffen detecteren ziekte door hartslagsignalen

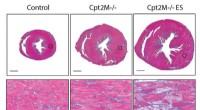
- Onderzoek toont aan dat vette brandstof nodig is om cardiale hypertrofie om te keren
- Onderzoekers maken doorbraak in lichtvangtechnologie voor industriële multikristallijne siliciumzonnecellen

- De olie uit vervuild water halen

- Nieuwe methode om kanker te bestrijden met moleculaire vezels
 Sex-ed is cruciaal voor de rechten van kinderen
Sex-ed is cruciaal voor de rechten van kinderen Wetenschappers ontdekken dat mechanisch gedrag van kleine structuren wordt beïnvloed door atoomdefecten
Wetenschappers ontdekken dat mechanisch gedrag van kleine structuren wordt beïnvloed door atoomdefecten Weer Weer lezen Radar
Weer Weer lezen Radar Wetenschappers gebruiken AI om nieuwe materialen voor koolstofafvang te identificeren
Wetenschappers gebruiken AI om nieuwe materialen voor koolstofafvang te identificeren  Nieuwe moleculaire printtechnologie kan complexe chemische omgevingen nabootsen die op het menselijk lichaam lijken
Nieuwe moleculaire printtechnologie kan complexe chemische omgevingen nabootsen die op het menselijk lichaam lijken Waarom is water belangrijk voor de landbouw?
Waarom is water belangrijk voor de landbouw?  Wat worden noorderlicht veroorzaakt door de zonnewind?
Wat worden noorderlicht veroorzaakt door de zonnewind?  Vier miljard deeltjes microplastics ontdekt in grote watermassa
Vier miljard deeltjes microplastics ontdekt in grote watermassa
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

