
Wetenschap
Welke elementen hebben dezelfde elektronenopstelling als argonchloorzwavel of kalium?
Inzicht in elektronenconfiguratie
* Elektronenconfiguratie: Dit beschrijft hoe elektronen zijn gerangschikt in de energieniveaus en sub -evers van een atoom.
* valentie -elektronen: Dit zijn de elektronen in het buitenste energieniveau, die betrokken zijn bij chemische binding.
* octetregel: Veel atomen streven ernaar om 8 valentie -elektronen (zoals de edelgassen) te hebben voor stabiliteit.
Analyse van de elementen
1. argon (AR): Argon heeft de elektronenconfiguratie 1S²2S²2P⁶3S²3P⁶. Het heeft een volledige buitenste schaal met 8 valentie -elektronen.
2. chloor (CL): Chloor heeft de elektronenconfiguratie 1S²2S²2P⁶3S²3P⁵. Het heeft 7 valentie -elektronen en heeft er nog een nodig om een octet te bereiken.
3. zwavel (s): Zwavel heeft de elektronenconfiguratie 1S²2S²2P⁶3S²3P⁴. Het heeft 6 valentie -elektronen en heeft er nog twee nodig om een octet te bereiken.
4. kalium (k): Kalium heeft de elektronenconfiguratie 1S²2S²2P⁶3S²3P⁶4S¹. Het heeft 1 valentie -elektron en verliest het gemakkelijk om de stabiele elektronenconfiguratie van argon te bereiken.
elementen met vergelijkbare configuraties
* argon (AR): Elementen in dezelfde groep (groep 18, edelgassen) hebben dezelfde elektronenregeling als argon. Voorbeelden zijn Neon (NE), Krypton (KR), Xenon (XE) en Radon (RN).
* chloor (CL): Elementen in dezelfde groep (groep 17, halogenen) hebben hetzelfde aantal valentie -elektronen als chloor en hebben er nog een nodig om een octet te bereiken. Voorbeelden zijn fluor (F), broom (BR), jodium (I) en astatine (AT).
* zwavel (s): Elementen in dezelfde groep (groep 16, chalcogenen) hebben hetzelfde aantal valentie -elektronen als zwavel en hebben er nog twee nodig om een octet te bereiken. Voorbeelden zijn zuurstof (O), Selenium (SE), Tellurium (TE) en Polonium (PO).
* kalium (k): Elementen in dezelfde groep (groep 1, alkali -metalen) hebben hetzelfde aantal valentie -elektronen als kalium, die er gemakkelijk een verliezen om een stabiele configuratie te bereiken. Voorbeelden zijn lithium (Li), natrium (NA), rubidium (RB), cesium (CS) en Francium (FR).
Samenvattend:
Elementen in dezelfde groep van de periodiek systeem hebben hetzelfde aantal valentie -elektronen en dus vergelijkbare elektronenregelingen. De edelgassen (zoals argon) hebben al een stabiel octet, terwijl andere elementen elektronen zullen winnen of verliezen om een vergelijkbare configuratie te bereiken.
 Hoe klimaatverandering nieuwe epidemieën aan het licht zou kunnen brengen
Hoe klimaatverandering nieuwe epidemieën aan het licht zou kunnen brengen  Het vuil op bodemverlies door de overstromingen in het Midwesten
Het vuil op bodemverlies door de overstromingen in het Midwesten Team ontdekt een belangrijke rol voor nitraat in het Arctische landschap
Team ontdekt een belangrijke rol voor nitraat in het Arctische landschap Dorian versterkt tot categorie 3 storm als het de oostkust van de VS bedreigt
Dorian versterkt tot categorie 3 storm als het de oostkust van de VS bedreigt Gevaarlijke hittegolven zullen de tropen waarschijnlijk dagelijks teisteren tegen 2100:studie
Gevaarlijke hittegolven zullen de tropen waarschijnlijk dagelijks teisteren tegen 2100:studie
Hoofdlijnen
- Hoe organiseren organen die verband houden met cellen en weefsels?
- Nieuwe bevindingen suggereren hoe en waarom temperaturen het geslacht van schildpadden bepalen
- Welke organel is verantwoordelijk voor het afbreken van vetzuren op suikers?
- Waarom kunnen de mutaties van Missenen geen effect hebben op de eiwitfunctie?
- Veertien jaar na de olieramp in de Golf van Mexico gaan de endemische vissen een onzekere toekomst tegemoet
- Wat is vaste macrofaag?
- Wat is het doel van de vrucht die zich ontwikkelt op een bloeiende plant?
- Evolueren organismen langzaam in de loop van de tijd en kunnen twee verschillende een gemeenschappelijke voorouder hebben?
- Zeesponzen bieden aanwijzingen hoe door de mens gemaakte structuren weerstand kunnen bieden aan knikken
- Het gebruik van schaaldieren bij het genezen van wonden - de toekomst van de geneeskunde?

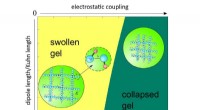
- Onderzoekers ontwikkelen microscopische theorie van polymeergel
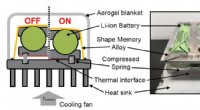
- Thermische oorkappen beschermen de batterijen van mobiele telefoons tegen extreme temperaturen
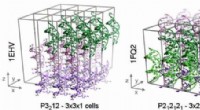
- Wetenschappers bereiken de eerste stabiele simulaties van DNA-kristallen
- Een milieuvriendelijke, goedkope oplossing voor afvalwaterzuivering

 Uw propaanmeter lezen was 25 Hoeveel gallons is dat?
Uw propaanmeter lezen was 25 Hoeveel gallons is dat?  Hoe de aarde warmte afgeeft aan de ruimte
Hoe de aarde warmte afgeeft aan de ruimte Wanneer is de zon direct boven Barbados?
Wanneer is de zon direct boven Barbados?  Controleerbare functionele ferro-elektrische domeinwanden onder piëzoresponsmicroscoop
Controleerbare functionele ferro-elektrische domeinwanden onder piëzoresponsmicroscoop Wat zijn de voordelen van voertuigen op waterstof?
Wat zijn de voordelen van voertuigen op waterstof?  Een stretchy mesh heater voor pijnlijke spieren
Een stretchy mesh heater voor pijnlijke spieren Onderzoekers ontdekken hoe met nectar beladen honingbijen oververhitting voorkomen
Onderzoekers ontdekken hoe met nectar beladen honingbijen oververhitting voorkomen  Waarom de kosten van het tegengaan van klimaatverandering niet kunnen worden teruggebracht tot één juist getal
Waarom de kosten van het tegengaan van klimaatverandering niet kunnen worden teruggebracht tot één juist getal
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

