
Wetenschap
Natrium- en chlooratomen combineren gemakkelijk omdat ze allebei de neiging hebben elektronen te verliezen.
* natrium (na) Heeft een enkel elektron in zijn buitenste schaal. Het heeft de neiging om te verliezen Dit elektron om een stabiele, volledige buitenste schaal te bereiken, die een positief geladen natriumion (Na+) vormt.
* chloor (Cl) heeft zeven elektronen in zijn buitenste schaal. Het heeft de neiging om te wonen Eén elektron om een stabiele, volledige buitenste schaal te bereiken, die een negatief geladen chloride-ion (Cl-) vormt.
De combinatie van natrium en chloor wordt aangedreven door de tegenovergestelde neigingen van de twee atomen:
* Natrium wil * een elektron verliezen.
* Chloor wil * een elektron winnen.
De elektrostatische aantrekkingskracht tussen het positief geladen natriumion en het negatief geladen chloride -ion vormt de ionische binding in natriumchloride (NaCl), algemeen bekend als tabelzout.
 Hoe wordt aardgas geproduceerd uit ruwe olie?
Hoe wordt aardgas geproduceerd uit ruwe olie?  Wat zijn alle producten van verbrandingszaken?
Wat zijn alle producten van verbrandingszaken?  Noem drie eigenschappen van metalen die het resultaat zijn van metaalbindingen?
Noem drie eigenschappen van metalen die het resultaat zijn van metaalbindingen?  Heterometallische koper-aluminium superatoom ontdekt
Heterometallische koper-aluminium superatoom ontdekt Hoe kunnen we zout-alkalibodems effectief verbeteren en gebruiken om de voedselzekerheid te garanderen?
Hoe kunnen we zout-alkalibodems effectief verbeteren en gebruiken om de voedselzekerheid te garanderen?
 Klimaatverandering maakt bouwen, visserij en andere gevaarlijke industrieën nog riskanter
Klimaatverandering maakt bouwen, visserij en andere gevaarlijke industrieën nog riskanter Lava verspreidt zich meer dan twee mijl van Filippijnse vulkaan
Lava verspreidt zich meer dan twee mijl van Filippijnse vulkaan Enquête peilt naar de mening van topleiders over het landschap van het milieubeleid
Enquête peilt naar de mening van topleiders over het landschap van het milieubeleid Digitale gegevens van bewaarde planten en dieren veranderen de manier waarop wetenschappers de wereld verkennen
Digitale gegevens van bewaarde planten en dieren veranderen de manier waarop wetenschappers de wereld verkennen  NASA vindt zware regenval in tropische storm Dorian
NASA vindt zware regenval in tropische storm Dorian
Hoofdlijnen
- Hoe de anatomie van een rundvleeshart en een menselijk hart te vergelijken
- Wetenschappers laten zien hoe parasieten bruine schaaldieren in moerassen in neonzombies veranderen
- Waar bestaan genen uit?
- Hoe zijn eetstokjes en wetenschap gerelateerd?
- Gebruiken alle vormen van leven aminozuren in DNA om genetische informatie op te slaan?
- Welke groep bevat het favoriete molecuul van de hersenen?
- Robotapparaat volgt plantengroei op cellulair niveau
- Wie zorgt er bij vogelkoppels voor de kinderen?
- Hoe de eenvoudige goudsbloem een verwoestende tomatenplaag te slim af is
- Onderzoekers ontdekken nieuwe moleculen voor het volgen van de ziekte van Parkinson
- Ontwerpbehandeling van geavanceerde metalen voor betere beeldhouwkunst

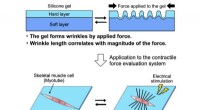
- Wetenschappers ontwikkelen directe meting voor kracht van skeletspiermyotubes
- MRI-scanning helpt bij batterijontwerp van de volgende generatie

- Bloedonderzoek kan de aanwezigheid van dodelijke superbacteriën in minder dan een uur detecteren

 Wat zijn twee soorten genetische drift?
Wat zijn twee soorten genetische drift?  SpaceX zegt maandag geen Starship-lancering
SpaceX zegt maandag geen Starship-lancering VN steunt Rusland bij internetverdrag, alarmerende voorstanders van rechten
VN steunt Rusland bij internetverdrag, alarmerende voorstanders van rechten Wetenschappers onthullen mechanisme van uitwisseling van elektronenladingen in moleculen
Wetenschappers onthullen mechanisme van uitwisseling van elektronenladingen in moleculen Naar welke bollen behoren de wolken?
Naar welke bollen behoren de wolken?  Hoe HP naar BTU /hr
Hoe HP naar BTU /hr Wat houdt de moleculen bij elkaar in vaste stof?
Wat houdt de moleculen bij elkaar in vaste stof?  Wat is het systeem van objecten rond de zon?
Wat is het systeem van objecten rond de zon?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

