
Wetenschap
Trokken of geeft chloor elektronen aan?
* elektronegativiteit: Chloor heeft een hoge elektronegativiteit, wat betekent dat het een sterke neiging heeft om elektronen naar zichzelf aan te trekken wanneer het chemische bindingen vormt.
* Elektronenconfiguratie: Chloor heeft zeven elektronen in zijn buitenste schaal. Het heeft nog een elektron nodig om een stabiele, volledige buitenste schaal te bereiken (zoals de edelgassen). Dit maakt het zeer reactief en enthousiast om een elektron te krijgen.
Voorbeelden:
* In een covalente binding met een minder elektronegatief element (zoals waterstof in HCl) zal chloor de gedeelde elektronen dichter bij zichzelf trekken, waardoor een gedeeltelijke negatieve lading op het chlooratoom ontstaat.
* Wanneer chloor reageert met een metaal (zoals natrium in NaCl), krijgt het een elektron van het metaal, waardoor een negatief geladen chloride -ion wordt gevormd (CL⁻).
Samenvattend: De sterke elektronegativiteit en elektronenconfiguratie van chloor maken het een elektronenacceptor, waardoor het wordt aangetrokken om elektronen aan te trekken in chemische reacties.
 Welke speciale aanpassingen moeten planten en dieren in droge regio's leven?
Welke speciale aanpassingen moeten planten en dieren in droge regio's leven?  Het Amerikaanse grondwater wordt zouter – wat dat betekent voor de infrastructuur, ecosystemen en de menselijke gezondheid
Het Amerikaanse grondwater wordt zouter – wat dat betekent voor de infrastructuur, ecosystemen en de menselijke gezondheid  Verzuring van de oceaan kan de visserij op zeeschelpen verminderen
Verzuring van de oceaan kan de visserij op zeeschelpen verminderen Hoe de natuurbescherming werkt
Hoe de natuurbescherming werkt  Carbon Cycling in Aquatic Ecosystems
Carbon Cycling in Aquatic Ecosystems
Hoofdlijnen
- Voedingsproduct op basis van schimmels dat smaakt en verscheurt als vlees
- Waar doen in de eukaryotische cel RNA -verwerking en translatie van replicatietranscriptie elk op?
- Kelp voor maïsgroei? Wetenschappers demystificeren gewassen van natuurlijke producten
- Welke organen beginnen met de letter c?
- Kunnen algen zowel aseksueel als seksueel reproduceren?
- Wat is de kleinste rattensoort?
- Zijn cytoplasma op planten of dieren?
- Wat is het molecuulgewicht van glucoseoxidase?
- Wat is het element dat het meest geassocieerd is met levende wezens en gevonden in alle vier macromoleculetypen?
- Onderzoek kan ongewenste bijwerkingen bij nieuwe medicijnen minimaliseren

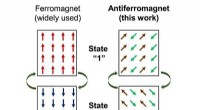
- Antiferromagnetische materialen grote stap richting commerciële toepassing
- Oorzaak van kathodedegradatie geïdentificeerd voor nikkelrijke materialen

- Nieuw proces voor volledig gebruik van zachthoutschors klaar voor productie

- Ultradunne roestlagen wekken elektriciteit op uit stromend water

 Post-tropische cycloon Prapiroons-resten bewegen over het noorden van Japan
Post-tropische cycloon Prapiroons-resten bewegen over het noorden van Japan COSINE-100-experiment onderzoekt mysterie van donkere materie
COSINE-100-experiment onderzoekt mysterie van donkere materie Is ammoniumhydroxide polair of niet -polair?
Is ammoniumhydroxide polair of niet -polair?  Op ferro-elektrisch grafeen gebaseerd systeem kan leiden tot verbeterde informatieverwerking
Op ferro-elektrisch grafeen gebaseerd systeem kan leiden tot verbeterde informatieverwerking De complexe kwestie van terugkerende strijders van de Islamitische Staat
De complexe kwestie van terugkerende strijders van de Islamitische Staat Moderne pygmeeën op het eiland Flores vertonen geen genetische link met uitgestorven hobbits
Moderne pygmeeën op het eiland Flores vertonen geen genetische link met uitgestorven hobbits Een wetenschappelijke benadering gebruiken om de waarde van reistijd te beoordelen
Een wetenschappelijke benadering gebruiken om de waarde van reistijd te beoordelen Wat is het verschil tussen echte Solar Day en Mean Day?
Wat is het verschil tussen echte Solar Day en Mean Day?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

