
Wetenschap
Is ammoniumhydroxide polair of niet -polair?
* stikstof en zuurstof: De stikstof- en zuurstofatomen in het molecuul zijn zeer elektronegatief, wat betekent dat ze elektronen sterker aantrekken dan waterstof.
* Polaire bindingen: De N-H en O-H-bindingen in het molecuul zijn polaire covalente bindingen vanwege het ongelijke delen van elektronen.
* Moleculaire geometrie: De algehele vorm van het ammoniumhydroxidemolecuul is asymmetrisch, wat bijdraagt aan de algehele polariteit. De dipoolmomenten van de polaire bindingen annuleren elkaar niet.
Belangrijke opmerking: Ammoniumhydroxide is eigenlijk een oplossing van ammoniak (NH₃) in water (H₂o). Ammoniak zelf is een polair molecuul vanwege het enige paar elektronen op het stikstofatoom. Wanneer het oplost in water, vormt het het ammoniumion (NH₄⁺) en hydroxide -ion (OH⁻), die beide ook polair zijn.
Laat het me weten als je nog andere vragen hebt!
 Heeft het wonen in de buurt van een olie- of aardgasbron invloed op uw drinkwater?
Heeft het wonen in de buurt van een olie- of aardgasbron invloed op uw drinkwater?  Moleculaire details van eiwit onthullen een glimp van hoe nierstenen zich vormen
Moleculaire details van eiwit onthullen een glimp van hoe nierstenen zich vormen Wat is de meest vluchtige chemische stof ter wereld?
Wat is de meest vluchtige chemische stof ter wereld?  Onderzoekers beschrijven structuren, mechanismen die bacteriën in staat stellen antibiotica te weerstaan
Onderzoekers beschrijven structuren, mechanismen die bacteriën in staat stellen antibiotica te weerstaan Nieuw materiaal op cellulosebasis vertegenwoordigt drie sensoren in één
Nieuw materiaal op cellulosebasis vertegenwoordigt drie sensoren in één
 Extreem weer zou ons misschien kunnen aanmoedigen om samen te werken aan de opwarming van de aarde
Extreem weer zou ons misschien kunnen aanmoedigen om samen te werken aan de opwarming van de aarde Kanpur voert WHO-zwarte lijst aan van steden met de ergste luchtvervuiling
Kanpur voert WHO-zwarte lijst aan van steden met de ergste luchtvervuiling Wetenschappers ontdekken 500 meter hoog koraalrif in het Great Barrier Reef, de eerste die in meer dan 120 jaar is ontdekt
Wetenschappers ontdekken 500 meter hoog koraalrif in het Great Barrier Reef, de eerste die in meer dan 120 jaar is ontdekt Hier leest u hoe Californië vuur kan gebruiken om het natuurbrandprobleem op te lossen
Hier leest u hoe Californië vuur kan gebruiken om het natuurbrandprobleem op te lossen  Estuaria warmen twee keer zo snel op als oceanen en atmosfeer
Estuaria warmen twee keer zo snel op als oceanen en atmosfeer
Hoofdlijnen
- Wat is een tyroid?
- Dit is een barrière voor reproductie bij een soort organismen, het resulteert vaak in genetische verandering in de loop van de tijd en de ontwikkeling van nieuwe soorten?
- Wat maakt sommige oesters veerkrachtiger dan andere?
- Wat is het verschil tussen zaden en sporen?
- Wat is een definitie van basis?
- Hebben mosasauriërs de schoolslag gedaan?
- Waren onze tetrapod-voorouders doof?
- Onderzoekers lossen het oude mysterie op over hoe fagen pathogene bacteriën ontwapenen
- Waarom cellen zure lysosomen nodig hebben
- Druppels beklimmen kan leiden tot efficiëntere waterwinning

- Ultrasone techniek onthult de identiteit van grafiet

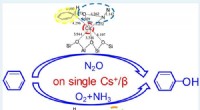
- Verbeterde katalytische processen voor de synthese van fenol
- Met metaaloxide doordrenkte membranen kunnen een energiezuinig alternatief bieden voor chemische scheidingen

- Ontwikkeling van cellulaire membraan-FET (lipid-FET) voor gevoeligheid van biosensor

 Welke kracht vormde de zonneplaneten en andere objecten uit deze nevel?
Welke kracht vormde de zonneplaneten en andere objecten uit deze nevel?  Wetenschappers ontwikkelen sensor om kinderen te redden huisdieren achtergelaten in voertuigen
Wetenschappers ontwikkelen sensor om kinderen te redden huisdieren achtergelaten in voertuigen Netflix en YouTube verlagen resolutie als virus op internet komt
Netflix en YouTube verlagen resolutie als virus op internet komt Nieuwe aanpak voor fotosynthetische productie van koolstofneutrale biobrandstof uit groene algen
Nieuwe aanpak voor fotosynthetische productie van koolstofneutrale biobrandstof uit groene algen Hoe het percentage te berekenen in Excel
Hoe het percentage te berekenen in Excel Afbeelding:de groene long van Bangkok
Afbeelding:de groene long van Bangkok Hoeveel waterstage zal een generator van 12 V 600 W produceren?
Hoeveel waterstage zal een generator van 12 V 600 W produceren?  Welke alkali wordt gebruikt om de zuurgraad van de bodem te verminderen?
Welke alkali wordt gebruikt om de zuurgraad van de bodem te verminderen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

