
Wetenschap
Wat vertelt het verhaal van een chemische reactie?
1. De chemische vergelijking:
* de meest elementaire en fundamentele manier om een reactie weer te geven. Het gebruikt symbolen om de reactanten (startmaterialen) en producten (resulterende stoffen) weer te geven, samen met hun stoichiometrische coëfficiënten (die de relatieve hoeveelheden van elk aangeven).
* Voorbeeld: 2H₂ + O₂ → 2H₂O (deze vergelijking vertelt ons dat twee moleculen waterstofgas reageren met één molecuul zuurstofgas om twee watermoleculen te produceren.)
* Beperkingen: Het toont alleen de algehele verandering, niet het stapsgewijze proces of de betrokken energie.
2. Het reactiemechanisme:
* beschrijft de volgorde van individuele stappen die optreden tijdens een reactie. Dit omvat de vorming van tussenproducten, het breken en vormen van bindingen en de activeringsenergieën van elke stap.
* Voorbeeld: De verbranding van methaan (CH₄) omvat verschillende stappen, waaronder de vorming van vrije radicalen en de afgifte van energie.
* Voordelen: Biedt een dieper inzicht in hoe de reactie verloopt.
3. Thermodynamica:
* richt zich op de energieveranderingen tijdens een reactie. Het maakt gebruik van concepten zoals enthalpie (warmteverandering), entropie (stoornis) en Gibbs -vrije energie om de haalbaarheid en spontaniteit van een reactie te voorspellen.
* Voorbeeld: De reactie tussen waterstof en zuurstof om water te vormen is exotherme, waardoor energie als warmte wordt vrijgeeft.
* Voordelen: Helpt voorspellen of een reactie zal plaatsvinden onder gegeven omstandigheden en de hoeveelheid vrijgegeven of geabsorbeerde energie.
4. Kinetiek:
* bestudeert de snelheid van een reactie. Het onderzoekt factoren die de reactiesnelheid beïnvloeden, zoals temperatuur, concentratie en katalysatoren.
* Voorbeeld: Het verhogen van de temperatuur van een reactie verhoogt typisch de reactiesnelheid als gevolg van hogere kinetische energie van de moleculen.
* Voordelen: Helpt de reactieomstandigheden te optimaliseren voor efficiëntie en controle.
5. Spectroscopische analyse:
* maakt gebruik van verschillende technieken om de reactanten en producten te analyseren, waardoor informatie over hun structuur en eigenschappen wordt verstrekt. Gemeenschappelijke technieken omvatten infrarood (IR) spectroscopie, nucleaire magnetische resonantie (NMR) spectroscopie en massaspectrometrie.
* Voorbeeld: IR -spectroscopie kan specifieke functionele groepen in een molecuul identificeren, waardoor de chemische veranderingen die tijdens een reactie plaatsvonden, kunnen begrijpen.
* Voordelen: Biedt gedetailleerde inzichten in de moleculaire transformaties die plaatsvinden tijdens de reactie.
6. Visualisaties en animaties:
* Gebruik 3D -modellen en animaties om het reactieproces op atomair en moleculair niveau weer te geven. Deze kunnen helpen de beweging van atomen, het breken en vormen van bindingen en de betrokken energieveranderingen te visualiseren.
* Voordelen: Biedt een meer intuïtief en boeiend begrip van de reactie.
Uiteindelijk wordt het "verhaal" van een chemische reactie verteld door informatie uit deze verschillende bronnen te combineren. Hoe meer informatie u verzamelt, hoe completer en genuanceerd dat uw begrip zal zijn.
 Met behulp van licht, rode bloedcellen en een honingbijpeptide om therapeutische eiwitten te leveren
Met behulp van licht, rode bloedcellen en een honingbijpeptide om therapeutische eiwitten te leveren Tot welke periode en groeps- en chemisch symbool behoren op het periodiek systeem?
Tot welke periode en groeps- en chemisch symbool behoren op het periodiek systeem?  Waarom kunnen luchtwater- en ijsbreuken in kleine fragmenten rotsen?
Waarom kunnen luchtwater- en ijsbreuken in kleine fragmenten rotsen?  Is CaSO4 ionisch of covalent gebonden?
Is CaSO4 ionisch of covalent gebonden?  Waarom leidt en tin corrodeen langzaam?
Waarom leidt en tin corrodeen langzaam?
Hoofdlijnen
- Wat wordt biologische evolutie gebruikt om uit te leggen?
- BESSY II werpt licht op hoe het interne kompas is opgebouwd in magnetotactische bacteriën
- Wat zijn voorbeelden van auxese?
- Hoe nuttig zijn microsatellieten?
- Wat zit er in elke geslachtscel?
- Wat is genetisch identiek en tegen elk bij centromere geactiveerd?
- Wat maakt bacteriën leven?
- Wie staat bekend als de vader van bacteriologie en protozoologie?
- Wat betekent het verzamelen van informatie in de wetenschap?
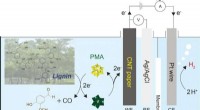
- Een nieuw biobrandstofsysteem voor waterstofproductie uit biomassa
- Polymeerprofessor ontwikkelt veiliger onderdeel voor lithiumbatterijen

- Chemici gebruiken elektrochemie om de productie van medicijnen te versterken

- Gigantische doorbraak in flexo-elektriciteit in zachte elastomeren maakt de weg vrij voor verbeterde robots en zelfaangedreven pacemakers

- Wetenschappers ontwikkelen lithium-ionbatterij die niet vlam vat

 Wat doet cellulaire ademhaling om het organisme ten goede te komen?
Wat doet cellulaire ademhaling om het organisme ten goede te komen?  Een nieuwe reeks doelen om de natuurlijke wereld te beschermen
Een nieuwe reeks doelen om de natuurlijke wereld te beschermen Inleiding tot hoe gigantische virussen werken
Inleiding tot hoe gigantische virussen werken  Hoe kom je bij de piramide van de zon?
Hoe kom je bij de piramide van de zon?  Klimaatbestendige broodvrucht is misschien wel het voedsel van de toekomst
Klimaatbestendige broodvrucht is misschien wel het voedsel van de toekomst Kwantumverstrengeling biedt ongekende precisie voor GPS en meer (Update)
Kwantumverstrengeling biedt ongekende precisie voor GPS en meer (Update) Waar betekent gespecialiseerde cellen?
Waar betekent gespecialiseerde cellen?  Wie oogst zonnen energie en produceert voedsel?
Wie oogst zonnen energie en produceert voedsel?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

