
Wetenschap
Elektronenconfiguratie van boor en zijn ion?
boron (b)
* Atomisch nummer: 5
* Elektronenconfiguratie: 1S² 2S² 2P¹
boor -ion (b³⁺)
* opladen: +3
* Elektronenconfiguratie: 1S²
Verklaring:
* Borons neutrale atoom: Boron heeft 5 elektronen, die zijn verdeeld in zijn elektronenschalen volgens het AUFBAU -principe en de heerschappij van Hund.
* De eerste schaal (n =1) kan maximaal 2 elektronen bevatten, dus deze is gevuld met 1S².
* De tweede schaal (n =2) kan maximaal 8 elektronen bevatten. Het begint met 2s², waardoor 1 elektron een van de 2p orbitalen heeft.
* boron ion (b³⁺): Boron verliest gemakkelijk zijn 3 buitenste elektronen (2s² 2p¹) om een stabiele, lege buitenste schaal te bereiken. Dit resulteert in een +3 lading en een configuratie die identiek is aan die van helium:1S².
 Welke verbindingen worden gevormd wanneer een kaars brandt?
Welke verbindingen worden gevormd wanneer een kaars brandt?  Het produceren van foutloze metaalkristallen van ongekende grootte
Het produceren van foutloze metaalkristallen van ongekende grootte Waarom moet een trechter worden verwarmd voordat hete acetanilide -oplossing is en gefilterd?
Waarom moet een trechter worden verwarmd voordat hete acetanilide -oplossing is en gefilterd?  Video:brandend ijs van de oceaanbodem
Video:brandend ijs van de oceaanbodem Wat zijn de zes soorten bewijs voor een chemische verandering?
Wat zijn de zes soorten bewijs voor een chemische verandering?
 Is de varen prothallus geschikt voor landomgeving die zoveel sporofyt is?
Is de varen prothallus geschikt voor landomgeving die zoveel sporofyt is?  Wat 'Tsjernobyl-honden' ons kunnen vertellen over overleven in vervuilde omgevingen
Wat 'Tsjernobyl-honden' ons kunnen vertellen over overleven in vervuilde omgevingen  Koelende rol van fijnstof bij opwarming aarde sterker dan eerder gedacht
Koelende rol van fijnstof bij opwarming aarde sterker dan eerder gedacht Wat is de volledige vorm van behoud?
Wat is de volledige vorm van behoud?  Dieren, geen droogte, de omgeving van onze voorouders gevormd
Dieren, geen droogte, de omgeving van onze voorouders gevormd
Hoofdlijnen
- Wat is een goede superheldennaam voor mobiel?
- Welk microscopisch dier leven in stof?
- Wat is de oorsprong van bot?
- Wat is een goede acrostische wetenschapszin?
- Wat is ongelijk verdeeld in de vrouwelijke cytokinese?
- Welke gamete wordt geproduceerd als één grote cel en drie kleinere cellen?
- Wat is de wetenschappelijke gemeenschappelijke naam voor gastro -intestinale ziekte?
- Wanneer groeit de cel en maakt hij een kopie van DNA?
- Wetenschappers hebben ontdekt dat de micro-inkapselingstechniek de efficiëntie van theeboomolie verhoogt voor duurzame toepassingen
- Onderzoekers suggereren dat RNA en DNA hun oorsprong hebben gevonden in RNA-DNA-chimeren
- Onderzoekers ontwikkelen computermodel om te voorspellen of een bestrijdingsmiddel schadelijk is voor bijen

- Wetenschappers ontdekken verbinding die zich richt op kankercellen die het beschermende p53-voogdgen missen
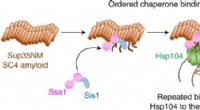
- Drie begeleiders coördineren het uiteenvallen van amyloïde fibrillen in gist
- Nieuwe productiemethode voor fullereenkristal 50 keer sneller dan zijn voorganger

 The Common Snakes of Oklahoma
The Common Snakes of Oklahoma  Hoe verschilt een niche van habitat?
Hoe verschilt een niche van habitat?  Welke term definieert de afstand tot een evenaar?
Welke term definieert de afstand tot een evenaar?  Elke ademhaling die je neemt:het traject volgen van de vervuiling door ingeademde plasticdeeltjes
Elke ademhaling die je neemt:het traject volgen van de vervuiling door ingeademde plasticdeeltjes  Filippijnse vulkaan braakt donkere pluim uit, dorpelingen geëvacueerd
Filippijnse vulkaan braakt donkere pluim uit, dorpelingen geëvacueerd Wat is bewijs dat grondwater erosie en afzetting veroorzaakt?
Wat is bewijs dat grondwater erosie en afzetting veroorzaakt?  Broadcom keert terug naar de VS
Broadcom keert terug naar de VS Angstaanjagende inzichten in klimaatverandering kunnen een wetgevend momentum creëren voor emissiereducties, onderzoekers beweren:
Angstaanjagende inzichten in klimaatverandering kunnen een wetgevend momentum creëren voor emissiereducties, onderzoekers beweren:
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

