
Wetenschap
Wat zijn de toeschouwersionen van AGC2H3O2 en CACL2?
1. Schrijf de gebalanceerde chemische vergelijking:
2 Agc₂h₃o₂ (aq) + cacl₂ (aq) → 2 agcl (s) + ca (c₂h₃o₂) ₂ (aq)
2. Identificeer de producten:
* zilveren chloride (AGCL): Dit is een vast neerslag, wat betekent dat het een vaste stof vormt en uit oplossing valt.
* calciumacetaat (ca (c₂h₃o₂) ₂): Dit blijft opgelost in oplossing als een waterige verbinding.
3. Bepaal de ionen die aanwezig zijn in oplossing voor en na de reactie:
Voor de reactie:
* agc₂h₃o₂ (aq): Ag⁺ (aq) + c₂h₃o₂⁻ (aq)
* cacl₂ (aq): Ca²⁺ (aq) + 2 cl⁻ (aq)
Na de reactie:
* agcl (s): Dit is een vaste stof en draagt niet bij aan de oplossing.
* ca (c₂h₃o₂) ₂ (aq): Ca²⁺ (aq) + 2 c₂h₃o₂⁻ (aq)
4. Identificeer de toeschouwersionen:
Toeschouwersionen zijn ionen die aan beide zijden van de vergelijking aanwezig zijn en niet deelnemen aan de reactie.
* ca²⁺ (aq) is aanwezig aan beide zijden van de vergelijking.
* c₂h₃o₂⁻ (aq) is aanwezig aan beide zijden van de vergelijking.
Daarom zijn de toeschouwersionen in deze reactie ca²⁺ en c₂h₃o₂⁻.
 Is worteltransplantatie een positief, coöperatief gedrag bij bomen?
Is worteltransplantatie een positief, coöperatief gedrag bij bomen?  NASA vangt nieuw gevormde tropische cycloon 11S
NASA vangt nieuw gevormde tropische cycloon 11S Als orkanen toeslaan, mensen zijn niet de enige slachtoffers
Als orkanen toeslaan, mensen zijn niet de enige slachtoffers Wat is het beste soort plantonderzoek voor een wetenschapsbeursproject?
Wat is het beste soort plantonderzoek voor een wetenschapsbeursproject?  Aanhoudende motregen bij temperaturen onder nul op Antarctica
Aanhoudende motregen bij temperaturen onder nul op Antarctica
Hoofdlijnen
- Wat is uniek aan de reproductie van Seahorse?
- Wat zijn de basisbehoeften van organismen?
- Waarom zijn alle levende organismen gegroepeerd in classificatiesystemen?
- Wat is een homologe structuur?
- Wat is het verschil in een virusfamilie en geslacht?
- Huisdieren of bedreigingen? Goudvissen kunnen schadelijk zijn voor de biodiversiteit
- Chinese wetenschappers onthullen een nieuwe signaalroute voor koude tolerantie in rijst
- De beste manier om de kosten voor het verwijderen van invasieve planten te schatten? Ga naar buiten en graaf
- VN schotelt vijgcactus voor als antwoord op voedselzekerheid
- Onderzoekers maken fotonische materialen voor krachtig, efficiënt op licht gebaseerd computergebruik

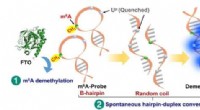
- Nieuwe sonde voor stofwisselingsziekten
- Wetenschappers krijgen atomistisch beeld van afbraak van platinakatalysator

- Wetenschappers gebruiken neutronen om te proberen zich beter te ontwikkelen, goedkopere tandheelkundige restauraties
- Ingenieur-kliniekteam gebruikt actieve rimpels om synthetische transplantaten schoon te houden

 Welke kostbare edelstenen zijn er te vinden in Texas?
Welke kostbare edelstenen zijn er te vinden in Texas?  Wat is de biosfeer waarin je leeft?
Wat is de biosfeer waarin je leeft?  Tweets blijken een betrouwbare indicator te zijn voor de luchtkwaliteit tijdens bosbranden
Tweets blijken een betrouwbare indicator te zijn voor de luchtkwaliteit tijdens bosbranden Wanneer een stuk palladiummetaal tot zeer fijn poeder wordt vermalen en verwarmd om eventueel atmosferisch vocht te verdrijven.
Wanneer een stuk palladiummetaal tot zeer fijn poeder wordt vermalen en verwarmd om eventueel atmosferisch vocht te verdrijven.  Waarom leidt een oplosbaar vast monster natriumzout geen elektriciteit?
Waarom leidt een oplosbaar vast monster natriumzout geen elektriciteit?  Klimaatverandering verandert de beschikbaarheid van terrestrisch water
Klimaatverandering verandert de beschikbaarheid van terrestrisch water Systeem om orgaantransplantatiemedicijn af te leveren - zonder schadelijke bijwerkingen
Systeem om orgaantransplantatiemedicijn af te leveren - zonder schadelijke bijwerkingen Welk genotype zou resulteren in bloedgroep A?
Welk genotype zou resulteren in bloedgroep A?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

