
Wetenschap
Hoe wordt chloride gemaakt?
Hier is een uitsplitsing van hoe chloride -ionen tot stand komen:
1. Natuurlijk voorkomend:
* Zeewater: De oceaan is de grootste bron van chloride -ionen en maakt ongeveer 1,9% van zijn massa uit. Chloride wordt gedurende miljoenen jaren opgelost uit rotsen en mineralen.
* rotsen en mineralen: Chloride is aanwezig in verschillende mineralen, zoals haliet (rotszout, NaCl), Sylvite (KCL) en carnalliet (kmgcl3 · 6h2o).
2. Chemische reacties:
* chloorgas (CL2): Chloorgas, een geelachtig groen gas, reageert gemakkelijk met veel stoffen om chloride-ionen te vormen. Dit proces is gebruikelijk in industriële toepassingen zoals de productie van zoutzuur (HCL).
* zoutzuur (HCl): Dit sterke zuur wordt gemaakt door waterstofchloridegas (HCL) in water op te lossen. HCL dissocieert in water om waterstofionen (H+) en chloride-ionen te vormen (Cl-).
3. Menselijke activiteiten:
* Industriële processen: Chloride -ionen worden geproduceerd als bijproducten in verschillende industriële processen, zoals de productie van kunststoffen, meststoffen en papier.
* Afvalwaterzuivering: Afvalwaterzuiveringsinstallaties gebruiken vaak chloor om water te desinfecteren, wat leidt tot de vorming van chloride -ionen.
4. Biologische processen:
* Levende organismen: Chloride -ionen zijn essentieel voor het leven. Ze spelen een cruciale rol bij het handhaven van vloeistofbalans, zenuwimpulsen en spiercontracties bij dieren.
Samenvattend:
Chloride -ionen zijn in de eerste plaats een natuurlijk voorkomend onderdeel van de omgeving. Ze worden gevormd door verschillende chemische reacties en biologische processen. Het "maken" van chloride -ionen verwijst vaak naar de specifieke processen waarmee chloride -ionen worden verkregen of gebruikt, maar ze zijn niet helemaal opnieuw gemaakt.
 Een lithiumatoom dat een elektron heeft verloren, komt in de buurt van een chloor gekregen elektron. Wat gebeurt er?
Een lithiumatoom dat een elektron heeft verloren, komt in de buurt van een chloor gekregen elektron. Wat gebeurt er?  Synthetische fysiologen ontwikkelen nieuwe receptor uitgeschakeld door groen licht
Synthetische fysiologen ontwikkelen nieuwe receptor uitgeschakeld door groen licht Nieuwe lijm voor betere recycling
Nieuwe lijm voor betere recycling Welke kleur krijgt waterstof van vochtig universeel indicatorpapier?
Welke kleur krijgt waterstof van vochtig universeel indicatorpapier?  Waarom verschillen verbindingen niet van mengsels?
Waarom verschillen verbindingen niet van mengsels?
 Soorten Pijlstaartrogvissen
Soorten Pijlstaartrogvissen Verandering van de vorm van valleien en dammen verandert het nitraatniveau van oppervlakte en grondwater op de schaal van het stroomgebied
Verandering van de vorm van valleien en dammen verandert het nitraatniveau van oppervlakte en grondwater op de schaal van het stroomgebied Blauwe bakken lopen over van Amazon- en Walmart-dozen. Maar waren eigenlijk minder aan het recyclen
Blauwe bakken lopen over van Amazon- en Walmart-dozen. Maar waren eigenlijk minder aan het recyclen Wat zijn de functies van Nephridia in regenwormen?
Wat zijn de functies van Nephridia in regenwormen?  Warmer worden? Het prehistorische klimaat kan toekomstige veranderingen helpen voorspellen
Warmer worden? Het prehistorische klimaat kan toekomstige veranderingen helpen voorspellen
Hoofdlijnen
- Van Zuidoost-Azië tot de riolen:studie bepaalt nieuwe geografische oorsprong van bruine ratten
- Wat zijn staafvormige bacteriën?
- Wat is H en O -antigenen?
- Wat is een Alektropia?
- Wat is een vetzuur? | Hoe dingen werken
- Wat is de grootte van nucleus met massanummer 216?
- Bij het analyseren van resultaten regelen wetenschappers soms gegevens in wat?
- Typen morfologie
- De aandelen van Facebook zinken, dus wie moet het kopen?
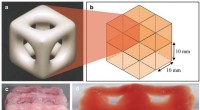
- 3D-printen creëert superzachte structuren die hersenen en longen nabootsen
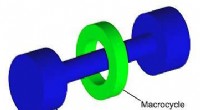
- Onderzoekers maken 's werelds snelste moleculaire shuttle
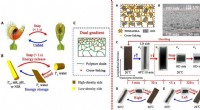
- Ontwikkeling van een ultrasnel biomimetisch snapping hydrogelmateriaal met twee gradiënten
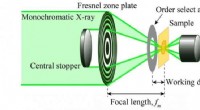
- Een scanning transmissie-röntgenmicroscoop voor analyse van chemische toestanden van lithium
- Van kegelslakkengif tot pijnverlichting

 Hoe de volgende generatie vliegtuigen ijsbestendig te maken?
Hoe de volgende generatie vliegtuigen ijsbestendig te maken? Het universum gebruiken als een kosmologische botser (update)
Het universum gebruiken als een kosmologische botser (update) Hoe insecten geuren opsporen door op microschaal winden te navigeren
Hoe insecten geuren opsporen door op microschaal winden te navigeren  Als algen uit de wateren verdwenen, hoe zouden andere levende wezens worden beïnvloed?
Als algen uit de wateren verdwenen, hoe zouden andere levende wezens worden beïnvloed?  Dodelijke bosbranden bereiken Turkse elektriciteitscentrale
Dodelijke bosbranden bereiken Turkse elektriciteitscentrale Is grafeen de beste kwantumweerstandsstandaard?
Is grafeen de beste kwantumweerstandsstandaard?  De acht dichtstbijzijnde planeet bij de zon?
De acht dichtstbijzijnde planeet bij de zon?  Online ruimte werkt niet als gelijkmaker voor vrouwelijke wetenschappers
Online ruimte werkt niet als gelijkmaker voor vrouwelijke wetenschappers
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

