
Wetenschap
Welk type binding bestaat tussen een atoomkoolstof en fluor?
Dit is waarom:
* elektronegativiteit: Fluor is het meest elektronegatieve element, wat betekent dat het een sterke aantrekkingskracht heeft op elektronen. Koolstof is ook elektronegatief, maar minder dan fluor.
* Elektronen delen: Vanwege dit elektronegativiteitsverschil delen koolstof- en fluor -elektronen om een stabiele binding te vormen. Beide atomen bereiken een volledige buitenste schaal van elektronen door te delen.
Hoewel de obligatie covalent is, is het belangrijk op te merken dat de gedeelde elektronen niet gelijk worden gedeeld. De elektronen worden sterker naar het fluoratoom getrokken, waardoor de binding polaire covalent is . Dit betekent dat de koolstof-fluorine-binding een gedeeltelijke negatieve lading heeft aan de fluorzijde en een gedeeltelijke positieve lading aan de koolstofzijde.
 Nieuwe aanpak van waterelektrolyse voor groene waterstof
Nieuwe aanpak van waterelektrolyse voor groene waterstof  Lost verdund zoutzuur koper op?
Lost verdund zoutzuur koper op?  Wat is het product van NaOH plus NH4Cl?
Wat is het product van NaOH plus NH4Cl?  Een virtueel substraat opent de weg naar oxidefilms op silicium voor toepassing in 5G, MEMS, sensoren en kwantumberekening
Een virtueel substraat opent de weg naar oxidefilms op silicium voor toepassing in 5G, MEMS, sensoren en kwantumberekening Is zuiveringszout oké om een hond zwavelboeren te laten verlichten?
Is zuiveringszout oké om een hond zwavelboeren te laten verlichten?
 De aarde onder Hawaï begrijpen
De aarde onder Hawaï begrijpen Effecten van autoverontreinigende stoffen op het milieu
Effecten van autoverontreinigende stoffen op het milieu Vraag van 500 miljard dollar:wat is de waarde van het bestuderen van de biologische koolstofpomp van de oceanen?
Vraag van 500 miljard dollar:wat is de waarde van het bestuderen van de biologische koolstofpomp van de oceanen? Wetgevers kondigen plan aan om Californische cap en trade uit te breiden
Wetgevers kondigen plan aan om Californische cap en trade uit te breiden Kleine stroompjes in agrarische ecosystemen zijn zwaar vervuild met pesticiden
Kleine stroompjes in agrarische ecosystemen zijn zwaar vervuild met pesticiden
Hoofdlijnen
- Hoe gedupliceerde genomen grassen hielpen te diversifiëren en bloeien
- Spechten vertonen tekenen van mogelijke hersenbeschadiging, maar dat is misschien geen slechte zaak
- Hoe heeft Griffith geholpen ons begrip van genetisch op te bouwen?
- Onderzoek toont aan waarom verdoving de wandelaars van cellen tegenhoudt
- Hebben gistcellen membraangebonden organellen?
- Waarom worden mensen niet beschouwd als goede organismen voor genetische studies?
- Hoe een dinosaurus te wegen
- M-fase: wat gebeurt er in deze fase van de celcyclus?
- Ingenieurs ontwerpen programmeerbare RNA-vaccins:tests op muizen laten zien dat ze werken tegen ebola, griep en veel voorkomende parasieten
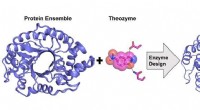
- Rise of the mutants:nieuw onderzoek om enzymontwerpmethodologieën te verbeteren
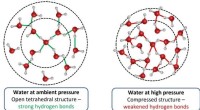
- Chemische stof in cellen van mariene organismen stelt hen in staat de hoge druk in diepe oceanen te overleven
- Onderzoekers ontwikkelen nieuwe chip voor superieure forensische detectie van bloedresten

- 3D-printen en maanstof:een astronautenkit voor toekomstige ruimteverkenning?

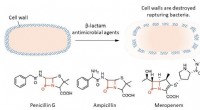
- Een nieuwe boosdoener in antibacteriële resistentie:cysteïnepersulfide
 Waarom beweegt Mercury Planet sneller rond de zon dan andere planeten?
Waarom beweegt Mercury Planet sneller rond de zon dan andere planeten?  Japan zoekt naar tientallen vermisten in modderstroom in badplaats
Japan zoekt naar tientallen vermisten in modderstroom in badplaats Wetenschappers beweren dat de huidige modellen voor klimaatverandering het probleem onderschatten
Wetenschappers beweren dat de huidige modellen voor klimaatverandering het probleem onderschatten Studie beschrijft hoe biomimetische nanomaterialen de schade na een hartaanval kunnen minimaliseren
Studie beschrijft hoe biomimetische nanomaterialen de schade na een hartaanval kunnen minimaliseren  De Ramanujan-machine:onderzoekers hebben een gissingengenerator ontwikkeld die wiskundige veronderstellingen creëert
De Ramanujan-machine:onderzoekers hebben een gissingengenerator ontwikkeld die wiskundige veronderstellingen creëert Wat is het verschil tussen de vastestoffysica en de gecondenseerde materiefysica?
Wat is het verschil tussen de vastestoffysica en de gecondenseerde materiefysica?  Waar gaat laserenergie heen nadat deze in plasma is geschoten?
Waar gaat laserenergie heen nadat deze in plasma is geschoten?  Protonen voeden de vooruitzichten voor grafeen
Protonen voeden de vooruitzichten voor grafeen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

