
Wetenschap
Waarom Copper 2 sulfaat geen elektriciteit in vaste toestand leidt?
* ionische structuur: Koper (II) sulfaat is een ionische verbinding, wat betekent dat het bestaat uit positief geladen koperionen (Cu²⁺) en negatief geladen sulfaationen (So₄²⁻). Deze ionen worden bij elkaar gehouden in een rigide, kristallijn rooster door sterke elektrostatische krachten.
* Geen gratis ladingsdragers: In de vaste toestand worden de ionen vastgelegd in hun posities in het kristalrooster. Ze kunnen niet vrij bewegen, dus er zijn geen mobiele ladingsdragers beschikbaar om een elektrische stroom te dragen.
Contrast dit met de gesmolten of opgeloste toestand:
* gesmolten toestand: Wanneer koper (II) sulfaat wordt gesmolten, breken de ionische bindingen en worden de ionen vrij om te bewegen. Dit zorgt voor de beweging van ladingsdragers en dus elektrische geleidbaarheid.
* Opgeloste toestand: In een waterige oplossing dissocieert koper (II) sulfaat in zijn ionen (Cu²⁺ en So₄²⁻), die vrij zijn om door de oplossing te bewegen. Deze beweging van ionen zorgt voor elektrische geleidbaarheid.
Samenvattend: De afwezigheid van vrije ladingsdragers in de vaste toestand van koper (II) sulfaat is de reden voor het gebrek aan elektrische geleidbaarheid. De ionen worden vergrendeld in een vaste positie in de kristallijne structuur, waardoor de stroom van elektriciteit wordt voorkomen.
 Zijn organische verbindingen vaste stoffen bij kamertemperatuur?
Zijn organische verbindingen vaste stoffen bij kamertemperatuur?  De lagen waardoor de ademhalingsgassen diffunderen, staan bekend als de?
De lagen waardoor de ademhalingsgassen diffunderen, staan bekend als de?  Water is een deel zuurstof en hoeveel delen waterstof?
Water is een deel zuurstof en hoeveel delen waterstof?  Welke van de volgende worden beschouwd als nobele gassen chloorbroom neon argon?
Welke van de volgende worden beschouwd als nobele gassen chloorbroom neon argon?  Nieuwe nanofotonische coating kan bijdragen aan thermisch beheer en contra-surveillance
Nieuwe nanofotonische coating kan bijdragen aan thermisch beheer en contra-surveillance
 Denk je dat de rampen van 2020 wild zijn? Experts zien erger in de toekomst
Denk je dat de rampen van 2020 wild zijn? Experts zien erger in de toekomst China ziet vier olievlekken van gezonken tanker
China ziet vier olievlekken van gezonken tanker Geleidbaarheidssleutel om water in de aarde in kaart te brengen
Geleidbaarheidssleutel om water in de aarde in kaart te brengen Grondwatervoorraden over de hele wereld kunnen tegen 2050 uitgeput zijn
Grondwatervoorraden over de hele wereld kunnen tegen 2050 uitgeput zijn Wetenschappers bestuderen hoe grootschalige verstoringen van het milieu oude samenlevingen beïnvloedden
Wetenschappers bestuderen hoe grootschalige verstoringen van het milieu oude samenlevingen beïnvloedden
Hoofdlijnen
- Hoe organiseren organen die verband houden met cellen en weefsels?
- Welk schip bevat sluitspier?
- Wat is een monomeer?
- Welke structuur in de hersenen speelt een rolaandrijving geassocieerd met het overleven van individu?
- Hebben dieren dezelfde vormcellen als een plant?
- Welke celonderdelen hebben plantcellen, maar dieren bevatten niet?
- Hoe wordt DNA-splitsing gebruikt in de biotechnologie?
- De Chinese bevolking krimpt opnieuw en zou meer dan kunnen halveren – dit is wat dat betekent
- Wat zijn de chemicaliën die instructies naar cellen sturen?
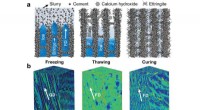
- Op hout geïnspireerd cement met hoge sterkte en multifunctionaliteit
- Laatste bevindingen over bittere stoffen in koffie
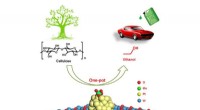
- Wetenschappers ontwikkelen een chemokatalytische benadering voor een-potreactie van cellulose-ethanol
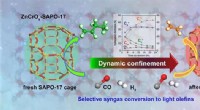
- Dynamische opsluiting van SAPO-17-kooien op selectiviteitscontrole van syngasconversie
- Een oplossing voor een harig probleem in de forensische wetenschap
 Natuurkundigen gebruiken hyperchaos om complexe kwantumsystemen te modelleren met een fractie van de rekenkracht
Natuurkundigen gebruiken hyperchaos om complexe kwantumsystemen te modelleren met een fractie van de rekenkracht Hoe kan een plastic zak groen zijn?
Hoe kan een plastic zak groen zijn?  Waarom brengen Red Dwarf -sterren de langste tijd door in de hoofdreeks?
Waarom brengen Red Dwarf -sterren de langste tijd door in de hoofdreeks?  Wat zijn twee fysische eigenschappen voor chroom?
Wat zijn twee fysische eigenschappen voor chroom?  De genetische afdruk van het paleolithicum is ontdekt in Noord-Afrikaanse populaties
De genetische afdruk van het paleolithicum is ontdekt in Noord-Afrikaanse populaties Hoe rocket neemt een wending in de ruimte?
Hoe rocket neemt een wending in de ruimte?  Zoeken naar zware nieuwe deeltjes met het ATLAS-experiment
Zoeken naar zware nieuwe deeltjes met het ATLAS-experiment Wat is de term voor zonnestraling die het oppervlak bereikt?
Wat is de term voor zonnestraling die het oppervlak bereikt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

