
Wetenschap
Hoe schrijf je zink reageert met waterig zoutzuur om II -chloride en waterstofgas te produceren?
Woordvergelijking:
Zink + zoutzuur → zinkchloride + waterstofgas
chemische vergelijking:
Zn (s) + 2HCl (aq) → ZnCl₂ (aq) + h₂ (g)
Verklaring:
* Zn (s): Zink is de vaste reactant.
* HCl (aq): Zoutzuur is de waterige reactant (opgelost in water).
* ZnCl₂ (aq): Zinkchloride is het waterige product (opgelost in water).
* h₂ (g): Waterstofgas is het gasvormige product.
het balanceren van de vergelijking:
De vergelijking is in evenwicht omdat er gelijke getallen van elk type atoom aan beide zijden van de vergelijking zijn:
* zink (Zn): 1 aan elke kant
* waterstof (h): 2 aan elke kant
* chloor (CL): 2 aan elke kant
Opmerking: De reactie is exotherme, wat betekent dat het warmte vrijgeeft, en je zou waarschijnlijk borrelen als waterstofgas wordt geproduceerd.
Hoofdlijnen
- Onderzoek onthult nieuwe aanwijzingen over hoe walvissen en dolfijnen echolocatie gingen gebruiken
- Hoe levende cellen een naald-in-hooiberg-probleem oplossen om elektrische signalen te produceren
- Wat is de logica van de wetenschap?
- Werkmodel over voedsellandbouw voor klasse 11e biologie?
- Kunnen vissen verkouden worden?
- Wat is de functie van chromosomen en centriolen?
- Wat is een antoniem van eiwitten?
- Welke levensfunctie is direct gerelateerd aan diffusie en osmose?
- Kunnen insecten dik worden?
- Wetenschappers ontwikkelen biorubberlijm voor sneller chirurgisch herstel en pijnverlichting
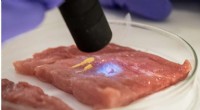
- Een komvormig gestructureerd ontwerp van een actieve site gebruiken om de schaalrelaties voor de omzetting van stikstof naar ammoniak te doorbreken
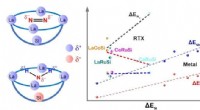
- Nieuwe geconsolideerde bio-saccharificatietechniek voor lignocelluloseconversie ontwikkeld
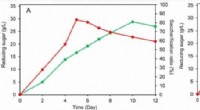
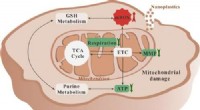
- Nanoplastics kunnen menselijke lever- en longcelprocessen verstoren in laboratoriumexperimenten
- Doping door atleten kan moeilijker te verbergen zijn met nieuwe detectiemethode
 Hoe virussen de manier veranderen waarop we naar evolutie kijken
Hoe virussen de manier veranderen waarop we naar evolutie kijken  Bepaal de volumeverandering die plaatsvindt wanneer een monster van 1,95 liter N2g wordt verwarmd van 250,0 K naar 442,2 K?
Bepaal de volumeverandering die plaatsvindt wanneer een monster van 1,95 liter N2g wordt verwarmd van 250,0 K naar 442,2 K?  Wat is interactie tussen de aarde en de zon?
Wat is interactie tussen de aarde en de zon?  Gezichtsbeschermers, maskers met kleppen niet effectief tegen verspreiding van COVID-19:studie
Gezichtsbeschermers, maskers met kleppen niet effectief tegen verspreiding van COVID-19:studie Waar bestaan morenen eigenlijk uit:klei en gesteente?
Waar bestaan morenen eigenlijk uit:klei en gesteente?  Is een 2 procent zoutoplossing hypertonisch of hypotonisch tot 4 oplossing?
Is een 2 procent zoutoplossing hypertonisch of hypotonisch tot 4 oplossing?  Waarom slimme kraai geen vogelbrein is
Waarom slimme kraai geen vogelbrein is  Twitter gaat gemanipuleerde inhoud, waaronder deepfakes, aan banden leggen
Twitter gaat gemanipuleerde inhoud, waaronder deepfakes, aan banden leggen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


