
Wetenschap
Wat is het percentage samenstelling van ammoniumcarbonaat?
1. Zoek de molaire massa van elk element:
* Stikstof (n):14,01 g/mol
* Waterstof (h):1,01 g/mol
* Koolstof (c):12.01 g/mol
* Zuurstof (O):16,00 g/mol
2. Bereken de molaire massa van ammoniumcarbonaat:
* (NH₄) ₂co₃:2 (14.01 g/mol + 4 (1,01 g/mol)) + 12,01 g/mol + 3 (16,00 g/mol) =96,09 g/mol
3. Bereken de massa van elk element in één mol ammoniumcarbonaat:
* Stikstof:2 * 14.01 g/mol =28,02 g/mol
* Waterstof:8 * 1,01 g/mol =8,08 g/mol
* Koolstof:12.01 g/mol
* Zuurstof:3 * 16.00 g/mol =48,00 g/mol
4. Bereken het percentage samenstelling van elk element:
* stikstof: (28,02 g/mol/96,09 g/mol) * 100% = 29,16%
* waterstof: (8,08 g/mol/96,09 g/mol) * 100% = 8,41%
* koolstof: (12,01 g/mol/96,09 g/mol) * 100% = 12,50%
* zuurstof: (48,00 g/mol/96,09 g/mol) * 100% = 50,00%
Daarom is het percentage samenstelling van ammoniumcarbonaat:
* stikstof:29,16%
* waterstof:8,41%
* koolstof:12,50%
* zuurstof:50,00%
 Vorig jaar was het bosbrandseizoen historisch voor West, maar Idaho ontsnapte. Hoe zit het met dit jaar?
Vorig jaar was het bosbrandseizoen historisch voor West, maar Idaho ontsnapte. Hoe zit het met dit jaar? Huis keurt wetgeving goed om chemische verontreiniging met PFAS aan te pakken
Huis keurt wetgeving goed om chemische verontreiniging met PFAS aan te pakken Vastgelopen weerpatronen zullen groter worden door klimaatverandering
Vastgelopen weerpatronen zullen groter worden door klimaatverandering Klimaatonderhandelaar waarschuwt wereld buiten tijd om eilanden te redden
Klimaatonderhandelaar waarschuwt wereld buiten tijd om eilanden te redden Snakes Found in Northern Illinois
Snakes Found in Northern Illinois
Hoofdlijnen
- We volgen al 18 jaar vogels in een klein Nigeriaans bos - wat we hebben gevonden en waarom het ertoe doet
- Eigenschappen die worden gevormd door veel genen die wat worden genoemd?
- Waarom gebruikt de genetica dieren voor hun erfelijkheidsexperimenten en niet mensen?
- Wat is een dier dat zich voedt met de lichamen van dode organismen?
- Honingbijen ultra-verbonden door hun microbioom
- Is de kernplaats van eiwitassemblage?
- Wat is de relatie tussen het ademhalingsproces en de cellulaire ademhaling?
- Is Blpharisma single of multi -cel?
- Wat is een organisme dat springt als er een fel licht naar scheen?
- Onderzoekers melden een nieuw en beter soort onzichtbare inkt

- structurele kleuren, zonder de glans

- Voeg gewoon water toe:een eenvoudige stap verhoogt het vermogen van polymeren om koolstofdioxide uit gemengde gassen te filteren

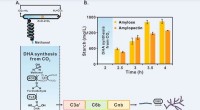
- Chinese wetenschappers rapporteren zetmeelsynthese uit koolstofdioxide
- Het nabootsen van het falen om de sterkte in composieten te vinden

 Mercurius zou de perfecte bestemming kunnen zijn voor een zonnezeil
Mercurius zou de perfecte bestemming kunnen zijn voor een zonnezeil  Kunststof elektronica met verflaag:polymeren uitlijnen voor hoge prestaties
Kunststof elektronica met verflaag:polymeren uitlijnen voor hoge prestaties Wat betekent de term die beschrijft hoe een mineraal licht van het oppervlak weerspiegelt?
Wat betekent de term die beschrijft hoe een mineraal licht van het oppervlak weerspiegelt?  Supercomputers helpen wetenschappers bij het bestuderen van de kleinste deeltjes in het universum
Supercomputers helpen wetenschappers bij het bestuderen van de kleinste deeltjes in het universum Het grootste deel van het hoekmomentum zonnestelsel is te vinden in de?
Het grootste deel van het hoekmomentum zonnestelsel is te vinden in de?  Heeft de temperatuur invloed op de hoeveelheid zout die oplost in water?
Heeft de temperatuur invloed op de hoeveelheid zout die oplost in water?  Hoeveel werk wordt er gedaan door een kracht van 500n op stationaire bakstenen muur?
Hoeveel werk wordt er gedaan door een kracht van 500n op stationaire bakstenen muur?  Wat zijn feiten over de wassende maansikkel?
Wat zijn feiten over de wassende maansikkel?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

