
Wetenschap
Wat zijn de chemische eigenschappen wanneer kaliumcarbonaat wordt toegevoegd aan HCL?
producten:
* koolstofdioxide (co₂): Dit gas wordt geproduceerd als bubbels en is verantwoordelijk voor de bruisen die in de reactie worden waargenomen.
* kaliumchloride (KCL): Dit is een oplosbaar zout dat in de oplossing blijft opgelost.
* water (h₂o): Dit wordt ook gevormd als een product van de reactie.
chemische vergelijking:
K₂co₃ (aq) + 2 HCl (aq) → 2 KCl (aq) + h₂o (l) + co₂ (g)
Verklaring:
* De reactie is een dubbele verplaatsingsreactie waar de positieve en negatieve ionen van de reactanten van plaats schakelen.
* Het carbonaation (co₃²⁻) reageert met de waterstofionen (H⁺) van HCl om carbonzuur te vormen (H₂co₃).
* Carbonzuur is onstabiel en ontleedt snel in koolstofdioxide (CO₂) en water (H₂o).
* De kaliumionen (k⁺) en chloride -ionen (CL⁻) blijven opgelost in de oplossing als kaliumchloride (KCL).
chemische eigenschappen:
* exotherme reactie: De reactie laat warmte vrij, waardoor de oplossing warm wordt.
* Gasevolutie: De vorming van kooldioxidegas is een karakteristieke observatie van deze reactie.
* neutralisatie: De reactie neutraliseert de zure eigenschappen van HCl.
* zoutvorming: Kaliumchloride, een zout, wordt geproduceerd als een product.
Veiligheidsmaatregelen:
* Voeg altijd langzaam en voorzichtig kaliumcarbonaat toe aan de zure oplossing om krachtig borrelen en potentiële spatten te voorkomen.
* Voer de reactie uit in een goed geventileerd gebied of gebruik een rookkap om te voorkomen dat koolstofdioxidegas inhaleert.
* Draag passende veiligheidsuitrusting, zoals bril en handschoenen.
 De temperatuur waarop een stof kookt, is een voorbeeld van fysieke eigenschap?
De temperatuur waarop een stof kookt, is een voorbeeld van fysieke eigenschap?  Nieuw algoritme helpt vergeten figuren onder Da Vinci-schilderij te ontdekken
Nieuw algoritme helpt vergeten figuren onder Da Vinci-schilderij te ontdekken Evenwichtige vergelijking voor koper II hydroxide verwarmd?
Evenwichtige vergelijking voor koper II hydroxide verwarmd?  De ontdekking van vloeibaar metaal luidt een nieuwe golf van chemie en elektronica in
De ontdekking van vloeibaar metaal luidt een nieuwe golf van chemie en elektronica in Wat is het verschil tussen verbinding en formule?
Wat is het verschil tussen verbinding en formule?
 Je stoot waarschijnlijk een verbazingwekkende hoeveelheid koolstofdioxide uit in je dagelijkse routine
Je stoot waarschijnlijk een verbazingwekkende hoeveelheid koolstofdioxide uit in je dagelijkse routine Dinosaurus-dodende asteroïde-impact koelde het klimaat op aarde meer af dan eerder werd gedacht
Dinosaurus-dodende asteroïde-impact koelde het klimaat op aarde meer af dan eerder werd gedacht Maximum categorie 5 orkaan Iota vaten richting Midden-Amerika
Maximum categorie 5 orkaan Iota vaten richting Midden-Amerika Methaanuitstoot uit reservoirs neemt toe
Methaanuitstoot uit reservoirs neemt toe Bosbranden val 2, 000 dorpelingen in Portugal
Bosbranden val 2, 000 dorpelingen in Portugal
Hoofdlijnen
- Hoe zijn ggo's gemaakt?
- 2 kiwivogels zijn zeldzaam lichtpuntje in grimmig uitstervingsrapport
- Een mogelijke verklaring voor hoe kiemlijnen worden verjongd
- Wat is de cellulaire immuunrespons?
- Wat zijn bloeiende sperma?
- Wat begint met F?
- Welke krachten vormen de Eaths -kenmerken?
- Wat zijn vragen, kan wetenschappers niet beantwoorden?
- Jackfruit uit de schappen laten springen
- Onderzoekers triggeren enzymen met licht
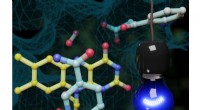
- Duurzamere mortels en beton met optimale thermische en mechanische efficiëntie

- Video:Brengen menselijke begrafenispraktijken de ecosystemen van de aarde in de war?

- Nieuwe methode versnelt simulaties, nieuwe inzichten geven in eiwitvouwing
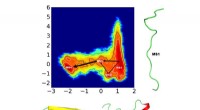
- Naar hoogwaardige mangaanoxidekatalysatoren met grote oppervlakten

 Hoe kun je een ster aan de hemel adopteren?
Hoe kun je een ster aan de hemel adopteren?  Onderzoek naar wat paren helpt om te gedijen, leert tieners over gezonde relaties
Onderzoek naar wat paren helpt om te gedijen, leert tieners over gezonde relaties  Metabolieten in algen cel voor cel meten
Metabolieten in algen cel voor cel meten Onderzoekers komen dichter bij praktische fotonische kwantumcomputers
Onderzoekers komen dichter bij praktische fotonische kwantumcomputers Waarom is de zon helderder dan de aarde?
Waarom is de zon helderder dan de aarde?  Netbetrouwbaarheid onder klimaatverandering vereist mogelijk meer capaciteit voor stroomopwekking
Netbetrouwbaarheid onder klimaatverandering vereist mogelijk meer capaciteit voor stroomopwekking Hoe Tangentallen in graden te converteren
Hoe Tangentallen in graden te converteren  Hoe zou u de waterstofbotsingsmachine beschrijven?
Hoe zou u de waterstofbotsingsmachine beschrijven?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

