
Wetenschap
Kijkend naar een gratis energiediagram voor een evenwichtsreactie Welke van de volgende scenario's zal de vorming meer reactant geven?
Gratis energiediagrammen
* vrije energie (g): De verticale as vertegenwoordigt de Gibbs -vrije energie van het systeem.
* Reactievoortgang: De horizontale as vertegenwoordigt de voortgang van de reactie, van reactanten links naar producten aan de rechterkant.
* overgangstoestand: De piek van het diagram vertegenwoordigt de overgangstoestand, het hoogste energiepunt tijdens de reactie.
* ΔG (verandering in vrije energie): Het verschil in vrije energie tussen reactanten en producten. Een negatieve Ag duidt op een spontane reactie die productvorming bevordert. Een positieve Ag duidt op een niet-spontane reactie die de vorming van reactant bevordert.
scenario's die de voorkeur geven aan reactanten
Hier zijn de scenario's die de vorming van meer reactanten in een evenwichtsreactie bevorderen, gebaseerd op een vrije energiediagram:
1. positieve ΔG (vrije energieverandering): Als de vrije energie van de producten hoger is dan de vrije energie van de reactanten (Ag is positief), is de reactie niet-spontaan. Dit betekent dat het systeem de reactanten zal bevoordelen.
2. Hoge activeringsenergie: Een zeer hoge activeringsenergie (het verschil in energie tussen de reactanten en de overgangstoestand) zal het voor de reactie moeilijk maken om verder te gaan. Dit vertraagt effectief de voorwaartse reactie, waardoor de reactanten de voorkeur hebben.
3. Groot verschil in vrije energie tussen reactanten en producten: Zelfs als de AG negatief is (voorkeur voor producten), zal een zeer groot verschil in vrije energie tussen reactanten en producten het evenwicht sterk naar de producten verschuiven. Dit betekent dat de evenwichtsconstante (k) erg groot zal zijn en de concentratie reactanten erg laag zal zijn.
Samenvattend:
* Een positieve ΔG bevordert altijd reactanten.
* Een hoge activeringsenergie kan de voorwaartse reactie belemmeren, die ook de voorkeur geeft aan reactanten.
* Een groot verschil in vrije energie tussen reactanten en producten, zelfs als ze negatief zijn, kan resulteren in zeer lage reactantconcentraties.
Voorbeeld:
Overweeg een reactie met een AG van +10 kJ/mol. Dit betekent dat de producten een hogere vrije energie hebben dan de reactanten. Het evenwicht zal zwaar liggen aan de zijkant van de reactanten.
Laat het me weten als je een specifiek voorbeeld wilt verkennen of nog vragen wilt hebben!
 Wat is een evenwichtige vergelijking voor de reactie van hydrazinevloeistof met zuurstofgas om stikstof en stoom te produceren?
Wat is een evenwichtige vergelijking voor de reactie van hydrazinevloeistof met zuurstofgas om stikstof en stoom te produceren?  Hoeveel atomen in siliciumtetrachloridemolecuul?
Hoeveel atomen in siliciumtetrachloridemolecuul?  Wat is de formule voor bariumhydride?
Wat is de formule voor bariumhydride?  Wat is een uitgebalanceerde chemische vergelijking, waarom zou deze in evenwicht moeten zijn?
Wat is een uitgebalanceerde chemische vergelijking, waarom zou deze in evenwicht moeten zijn?  Effecten van chloorinhalatie
Effecten van chloorinhalatie
 Giftige afvoer van de Tijuana-rivier valt Imperial Beach binnen
Giftige afvoer van de Tijuana-rivier valt Imperial Beach binnen De elektriciteitssector in Australië moet de CO2-uitstoot tegen 2030 met 45% verminderen
De elektriciteitssector in Australië moet de CO2-uitstoot tegen 2030 met 45% verminderen Spuitbussen voegen een nieuwe rimpel toe aan klimaatverandering in de tropische Stille Oceaan
Spuitbussen voegen een nieuwe rimpel toe aan klimaatverandering in de tropische Stille Oceaan Hoe een babyvogel als een kardinaal te identificeren
Hoe een babyvogel als een kardinaal te identificeren Klimaat in gematigde graslanden
Klimaat in gematigde graslanden
Hoofdlijnen
- Update over bedreigde Filippijnse cycadsoorten
- Invasieve soorten reptielen en amfibieën veroorzaken wereldwijd miljarden dollars aan schade
- Waarom is classificatie belangrijk voor ecologen?
- Wat is de methode waarmee tropische en niet-tropische hormonen een respons veroorzaken?
- Het verschil tussen een sporofyt en gametofyt
- Wat is de cellulaire diversiteit?
- Hoe een enzym in vuurvliegjes, klikkevers en glimwormen verschillende kleuren oplevert
- Hoe een mug te vangen
- Welk dubbele membraanorganel beschermt DNA?
- Principes voor een groene chemietoekomst

- Studie onthult geheim 18e-eeuws portret

- waren heet, vochtige zomers de sleutel tot de oorsprong van het leven?
- Wat is het verschil tussen relatieve vochtigheid en dauwpunt?

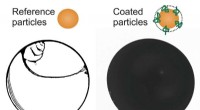
- Het modificeren van oppervlakken met polymeerketens bevordert een gelijkmatige droging van deeltjesbevattende vloeistoffen
 Als kristalzout een massa van 0,12 g heeft, hoeveel NaCl -formule -eenheden heeft het?
Als kristalzout een massa van 0,12 g heeft, hoeveel NaCl -formule -eenheden heeft het?  Chinese techgigant buitenspel gezet, Invoer VS gehouden te midden van handelsruzie
Chinese techgigant buitenspel gezet, Invoer VS gehouden te midden van handelsruzie Welke twee dingen zijn nodig voor cellen om energie te krijgen?
Welke twee dingen zijn nodig voor cellen om energie te krijgen?  The Physics of Music: Waves, Beats & Frequencies
The Physics of Music: Waves, Beats & Frequencies  Waarom is het centrum van een zonnevlek donker?
Waarom is het centrum van een zonnevlek donker?  Welk land bevindt zich 10 graden North en 61 West?
Welk land bevindt zich 10 graden North en 61 West?  Als de wereld niet genoeg is - hoe vind je een andere planeet om op te leven?
Als de wereld niet genoeg is - hoe vind je een andere planeet om op te leven? Waarom gebruik je galvanometer?
Waarom gebruik je galvanometer?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

