
Wetenschap
Wat is een indicatorzuur of alkali?
Hier is hoe het werkt:
* zure oplossingen: Indicatoren draaien één kleur in zure oplossingen, die een pH hebben die lager zijn dan 7.
* Basic (alkaline) oplossingen: Indicatoren draaien een andere kleur in basisoplossingen, die een pH hebben hoger dan 7.
* Neutrale oplossingen: Indicatoren kunnen een heel andere kleur hebben in neutrale oplossingen, die een pH van 7 hebben.
Voorbeelden van indicatoren:
* Litmus -papier: Wordt rood in zure oplossingen en blauw in basisoplossingen.
* fenolftalein: Kleurloos in zure oplossingen en roze in basisoplossingen.
* methylsinaasappel: Rood in zure oplossingen en geel in basisoplossingen.
* Bromothymol Blue: Geel in zure oplossingen, blauw in basisoplossingen en groen in neutrale oplossingen.
Hoe indicatoren werken:
Indicatoren zijn meestal zwakke zuren of basen zelf. Wanneer ze reageren met een zuur of base, verandert hun moleculaire structuur, waardoor een verschuiving in hun lichtabsorptie -eigenschappen veroorzaakt, die we beschouwen als een kleurverandering.
Belang van indicatoren:
* titratie: Indicatoren zijn cruciaal in titratie -experimenten, waarbij ze het eindpunt van een reactie aangeven door van kleur te veranderen.
* pH -meting: Indicatoren bieden een visuele manier om de zuurgraad of alkaliteit van een oplossing te beoordelen.
* Chemie -opleiding: Indicatoren worden gebruikt in laboratoriumdemonstraties om studenten te leren over zuren, basen en pH.
Laat het me weten als je nog meer vragen hebt!
 Preseismische atmosferische radonanomalie geassocieerd met aardbeving in Noord-Osaka in 2018
Preseismische atmosferische radonanomalie geassocieerd met aardbeving in Noord-Osaka in 2018 NASA ziet de zwaarste regenval in tropische cycloon Calebs
NASA ziet de zwaarste regenval in tropische cycloon Calebs NASA vindt orkaan Marie snel heviger
NASA vindt orkaan Marie snel heviger Wat klimaatactivisten kunnen leren van First Nations-campagnes tegen de fossiele brandstofindustrie
Wat klimaatactivisten kunnen leren van First Nations-campagnes tegen de fossiele brandstofindustrie Het VK verspilt elk jaar miljoenen tonnen voedsel - hier kunnen we verandering in brengen
Het VK verspilt elk jaar miljoenen tonnen voedsel - hier kunnen we verandering in brengen
Hoofdlijnen
- Welk lichaamssysteem is verantwoordelijk voor thermoregulatie?
- Hoe structuur en functie gerelateerd?
- Hoe ontwikkelen pathogenen nieuwe virulentie-activiteiten, en waarom doet dat ertoe?
- Welke van de volgende technologieën opende een nieuwe takwetenschap in de jaren 1970 A. Lichtmicroscoop B. Veranderende genen Bacteriën C. Centrifuge D. Chromatografie?
- Wat is een voorbeeld van postzygotische isolatie?
- Wat reist van je hersenen naar skeletspiercellen als je beweegt?
- Tegelijkertijd inzoomen door tijd en ruimte met superresolutie om te begrijpen hoe cellen zich delen
- Wat is de relatie tussen een chromosoom en een allel?
- Kan een schimmelinfectie wormen laten groeien?
- Virulentiefactor van het influenza A-virus in realtime in kaart gebracht
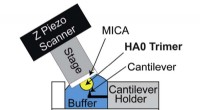
- Toolkit:lokale grond gebruiken voor 3D-printen van grote structuren

- Kan kunstmatige intelligentie nieuwe deuren openen voor het ontdekken van materialen?

- Een mechanisme voor het ontwerpen van legeringen met hoge entropie met verbeterde magnetische eigenschappen

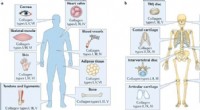
- Onderzoekers kwantificeren, karakteriseren en identificeren functies van collageen, zijn subtypes
 NASA's Psyche-missie heeft een metalen wereld in het vizier
NASA's Psyche-missie heeft een metalen wereld in het vizier Hoe heet een reactie tussen zuur en base?
Hoe heet een reactie tussen zuur en base?  Wanneer gebruik je de gemiddelde snelheid om te meten?
Wanneer gebruik je de gemiddelde snelheid om te meten?  Onderzoekers ontwikkelen een pad naar vloeibare zonnecellen die op oppervlakken kunnen worden geprint
Onderzoekers ontwikkelen een pad naar vloeibare zonnecellen die op oppervlakken kunnen worden geprint Canadese regering streeft naar koolstofneutraliteit tegen 2050
Canadese regering streeft naar koolstofneutraliteit tegen 2050 Nieuwe strategieën voor het ontwerpen van elektroluminescente materialen
Nieuwe strategieën voor het ontwerpen van elektroluminescente materialen Hoe overleef je een tactische atoombom? Defensie-experts leggen uit
Hoe overleef je een tactische atoombom? Defensie-experts leggen uit Onderzoek onderzoekt de staat van bescherming van migrerende werknemers
Onderzoek onderzoekt de staat van bescherming van migrerende werknemers
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

