
Wetenschap
Wat gebeurt er als vaste stoffen en vloeistoffen worden verwarmd of gekoeld?
Verwarming
* vaste stoffen:
* Verhoogde kinetische energie: Het verwarmen van een vaste stof zorgt ervoor dat de deeltjes erin sneller trillen en met een grotere amplitude. Deze verhoogde kinetische energie duwt de deeltjes verder uit elkaar, wat leidt tot:
* Uitbreiding: De vaste stof breidt zich in grootte uit. Denk aan een metalen staaf die langer wordt wanneer hij wordt verwarmd.
* staatsverandering (smelten): Als er voldoende warmte wordt toegevoegd, zullen de deeltjes uiteindelijk de krachten overwinnen die ze in een vaste structuur houden. Dit is wanneer de vaste stof verandert in een vloeistof (smelten).
* vloeistoffen:
* Verhoogde kinetische energie: Net als vaste stoffen, laat het verwarmen van een vloeistof de deeltjes sneller bewegen.
* Uitbreiding: Vloeistoffen breiden ook uit wanneer het wordt verwarmd. Daarom vul je een theepot iets minder dan vol, anticiperend op de uitbreiding van het water.
* staatsverandering (koken): Als de vloeistof wordt verwarmd tot voldoende temperatuur, krijgen de deeltjes voldoende energie om los te breken van het oppervlak van de vloeistof en een gas te worden (koken).
koeling
* vaste stoffen:
* Verminderde kinetische energie: Wanneer gekoeld, vertraagt de deeltjes in een vaste stof en trillen ze minder.
* samentrekking: Naarmate de deeltjes dichter bij elkaar komen, contracten in grootte.
* vloeistoffen:
* Verminderde kinetische energie: Het afkoelen van een vloeistof laat zijn deeltjes langzamer bewegen.
* samentrekking: Vloeistoffen samentrekken ook wanneer ze zijn afgekoeld.
* staatsverandering (bevriezen): Als de vloeistof voldoende wordt afgekoeld, vertragen de deeltjes tot het punt waar ze in een vaste structuur worden gehouden, die overstappen van een vloeistof naar een vaste stof (bevriezen).
Sleutelpunten:
* Temperatuur en kinetische energie: Temperatuur is een maat voor de gemiddelde kinetische energie van deeltjes. Hoe heter iets is, hoe sneller zijn deeltjes bewegen.
* intermoleculaire krachten: De sterkte van de krachten die de deeltjes bij elkaar houden (intermoleculaire krachten) bepaalt hoeveel energie nodig is om de toestand van materie te veranderen.
* Uitzonderingen: Sommige materialen gedragen zich anders. Water breidt bijvoorbeeld uit wanneer het bevriest, en daarom zweeft ijs.
Laat het me weten als je wilt dat ik een specifiek aspect uitgewerkt!
 Wat is het verschil tussen molaire massa en molecuulgewicht?
Wat is het verschil tussen molaire massa en molecuulgewicht?  Waar zijn de eigenschappen van compound van afhankelijk?
Waar zijn de eigenschappen van compound van afhankelijk?  Kun je koperchloride opslaan in een ijzeren vat?
Kun je koperchloride opslaan in een ijzeren vat?  De kracht van pauze:gecontroleerde afzetting voor effectieve en langdurige organische apparaten
De kracht van pauze:gecontroleerde afzetting voor effectieve en langdurige organische apparaten  Onderzoek vooruitgang zoeken naar nieuwe antibiotica
Onderzoek vooruitgang zoeken naar nieuwe antibiotica
 Sri Lanka vecht tegen golven plastic afval van brandend schip
Sri Lanka vecht tegen golven plastic afval van brandend schip 2050 is te laat - we moeten de uitstoot veel eerder drastisch verminderen
2050 is te laat - we moeten de uitstoot veel eerder drastisch verminderen Laat roet van bosbranden een stempel achter op de oceanen van de wereld?
Laat roet van bosbranden een stempel achter op de oceanen van de wereld? Venetië is niet alleen:7 zinkende steden over de hele wereld
Venetië is niet alleen:7 zinkende steden over de hele wereld  NASA ziet ex-tropische cycloon Debbie boven Queensland
NASA ziet ex-tropische cycloon Debbie boven Queensland
Hoofdlijnen
- Wetenschappers ontdekken waarom rijp fruit gevoeliger is voor necrotrofe ziekteverwekkers dan onrijp fruit
- Wat zijn de drie criteria waarnaar Thomas Hunt Morgan zocht in genetische studies naar modelorganismen?
- Algen en meercellige planten zijn autotrofen omdat ze?
- Hoe evolutie werkt
- Hoe kan osmose worden beschouwd als het samensmelten van water door een membraan?
- Hoe biofilms in de ruimte onder controle te houden
- Hoe zijn de producten van fotosynthese gerelateerd aan celademhaling?
- AI kan onderzoekers helpen begrijpen wat virussen van plan zijn in de oceanen en in uw darmen
- Wat is een biologisch gevaarlijk materiaal?
- Een TRAP instellen voor pandemische virussen

- Ferrofluide oppervlaktesimulaties gaan verder dan alleen de huid

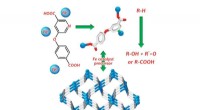
- Chemicus synthetiseert ijzercoördinatiepolymeer met nicotinezuurderivaat
- Morsen in een nucleaire faciliteit toont potentiële brandwondenrisico's van een huishoudelijke chemische stof

- Synthesestudies transformeren afvalsuiker voor toepassingen voor duurzame energieopslag
 Klimaatwetenschappelijk rapport cruciaal voor succes van COP26:UN
Klimaatwetenschappelijk rapport cruciaal voor succes van COP26:UN Coronavirus en de impact ervan op de CO2-uitstoot
Coronavirus en de impact ervan op de CO2-uitstoot Nieuwe moleculaire val reinigt meer radioactief afval van splijtstofstaven
Nieuwe moleculaire val reinigt meer radioactief afval van splijtstofstaven Berekening van de totale productiefunctie
Berekening van de totale productiefunctie Wat is de volgende stap als een experiment uw bevestiging van uw hypothese niet bevestigt?
Wat is de volgende stap als een experiment uw bevestiging van uw hypothese niet bevestigt?  Afvalwarmte omzetten in waterstofbrandstof
Afvalwarmte omzetten in waterstofbrandstof Hoe organisaties giftige werkplekculturen kunnen aanpakken om seksuele intimidatie aan te pakken
Hoe organisaties giftige werkplekculturen kunnen aanpakken om seksuele intimidatie aan te pakken  Welke planeten draaien rond de zon?
Welke planeten draaien rond de zon?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

