
Wetenschap
Welke vaste stoffen lossen op in water om een kleurloze oplossing te vormen?
ionische verbindingen:
* zouten: Meest voorkomende tafelzout (NaCl), kaliumchloride (KCL), natriumbromide (NABR), magnesiumsulfaat (MgSO4), enz.
* eenvoudige zuren: Zoutzuur (HCL), salpeterzuur (HNO3), zwavelzuur (H2SO4), enz.
* eenvoudige bases: Natriumhydroxide (NaOH), kaliumhydroxide (KOH), enz.
Covalente verbindingen:
* suikers: Sucrose (tafel suiker), glucose, fructose, etc.
* alcoholen: Ethanol (alcohol drinken), methanol, etc.
* Sommige gassen: Koolstofdioxide (CO2), ammoniak (NH3) - Deze vormen zwakke oplossingen met water.
Belangrijke opmerking: Kleurloos betekent niet dat de oplossing puur water is. Veel opgeloste stoffen zijn kleurloos, maar dragen bij aan de eigenschappen van de oplossing.
Uitzonderingen:
* Sommige verbindingen vormen gekleurde oplossingen: Kopersulfaat (CUSO4) vormt een blauwe oplossing, kaliumpermanganaat (kmno4) vormt een paarse oplossing.
* Sommige vaste stoffen kunnen oplossen om een bewolkte oplossing te vormen: Dit gebeurt vaak met onoplosbare stoffen, waar kleine deeltjes blijven gesuspendeerd, of met vaste stoffen die neerslag vormen.
Om te bepalen of een specifieke vaste stof een kleurloze oplossing zal vormen, moet u de oplosbaarheid en kleureigenschappen opzoeken.
 Het proces waarbij water verandert in vloeistof wordt genoemd?
Het proces waarbij water verandert in vloeistof wordt genoemd?  Sub-nanodeeltjeskatalysatoren gemaakt van muntelementen als effectieve katalysatoren
Sub-nanodeeltjeskatalysatoren gemaakt van muntelementen als effectieve katalysatoren Onderzoek onthult op nikkel gebaseerde katalysatoren met opmerkelijke economische haalbaarheid
Onderzoek onthult op nikkel gebaseerde katalysatoren met opmerkelijke economische haalbaarheid  Hoe berekent u de concentratie van xanthofyl op ethanol?
Hoe berekent u de concentratie van xanthofyl op ethanol?  Wetenschappers gebruiken gemodificeerde zijde-eiwitten om nieuwe anti-aanbakoppervlakken te creëren
Wetenschappers gebruiken gemodificeerde zijde-eiwitten om nieuwe anti-aanbakoppervlakken te creëren
Hoofdlijnen
- Welk cellichaam produceert?
- Wat is een lichaamsfossiel?
- Barsten plantencellen uit als het in zoet water wordt gedaan?
- De gamete die haploïde vorm van de groene alga -ulva produceert, staat bekend als een?
- Verschillen tussen Protista & Monera
- Wat zou het onderdeel van complementair DNA zijn dat wordt geproduceerd door onderstaande tcg aagask ons iets?
- Wat is de tak van zoölogie die wolven bestudeert?
- In welke fase condenseert chromosomen en worden ze zichtbaar?
- Hoe ziet het zaad van Gerbera eruit?
- Meervoudige aanval van virussen op bacteriën wijst op nieuwe manieren om infecties te bestrijden
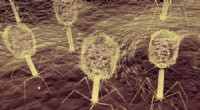
- Verankerd door een dichte buurt:wat voorkomt dat cellen afdwalen?

- Verbeterde fotosynthese van ammoniak in de omgeving met behulp van nanosheets met lichtschakelbare zuurstofvacatures
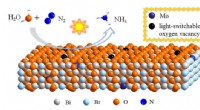
- Wetenschappers onthullen hoe wasmiddelen eigenlijk werken
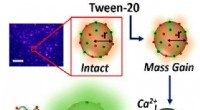
- Een snelle, gebruiksvriendelijke DNA-amplificatiemethode bij 37 Celsius

 Wat is een functie gevormd door zijrivier?
Wat is een functie gevormd door zijrivier?  Nieuw camerasysteem om beelden en video's met hoge resolutie van maanlandingen te bieden
Nieuw camerasysteem om beelden en video's met hoge resolutie van maanlandingen te bieden Hoe Twitter – nu X – helpt bij het begrijpen van de Canadese waarden en houding ten opzichte van asielzoekers
Hoe Twitter – nu X – helpt bij het begrijpen van de Canadese waarden en houding ten opzichte van asielzoekers  Hoe kwam de zon in het midden van Solar Systym?
Hoe kwam de zon in het midden van Solar Systym?  Licht laat elektronen ontsporen door grafeen
Licht laat elektronen ontsporen door grafeen Wat is een voorbeeld van algemene met specifieke analogie?
Wat is een voorbeeld van algemene met specifieke analogie?  Niet-duurzame bodemerosie in delen van het VK
Niet-duurzame bodemerosie in delen van het VK Wat is de bron van stralingswarmte?
Wat is de bron van stralingswarmte?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

